
ЁОЬтФПЁПвбжЊЯТСаЪЕбщЪТЪЕЃК
ЂйCr2O3ЙЬЬхМШФмШмгкKOHШмвКЕУЕНKCrO2ШмвКЃЌгжФмШмгкСђЫсЕУЕНCr2(SO4)3ШмвКЃЛ
ЂкЯђKCrO2ШмвКжаЕЮМгH2O2ШмвКЃЌдйЫсЛЏЃЌПЩЕУK2Cr2O7ШмвКЃЛ
ЂлНЋK2Cr2O7ШмвКЕЮМгЕНЕэЗлКЭKIЕФЛьКЯШмвКжаЃЌШмвКБфРЖЁЃ
ЯТСаХаЖЯВЛе§ШЗЕФЪЧ( )
AЃЎЛЏКЯЮяKCrO2жаCrдЊЫиЮЊЃЋ3Мл
BЃЎЪЕбщЂйжЄУїCr2O3ЪЧСНадбѕЛЏЮя
CЃЎЪЕбщЂкжЄУїH2O2МШгабѕЛЏадгжгаЛЙдад
DЃЎЪЕбщЂлжЄУїбѕЛЏадЃКCr2O![]() >I2
>I2
ЁОД№АИЁПC
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКAЁЂЛЏКЯЮяKCrO2жаЃЌKЮЊ+1МлЃЌOЮЊ-2МлЃЌгЩЛЏКЯЮяжае§ИКЛЏКЯМлЕФЕЙЪ§КЭЮЊ0ЃЌдђCrдЊЫиЮЊ+3МлЃЌе§ШЗЃЛBЁЂгЩЗДгІЂйПЩжЊЃЌбѕЛЏИѕгыЫсЁЂМюЗДгІЩњГЩбЮКЭЫЎЃЌЮЊСНадбѕЛЏЮяЃЌе§ШЗЃЛCЁЂЪЕбщЂкжаЗЂЩњбѕЛЏЛЙдЗДгІЃЌCrдЊЫиЕФЛЏКЯМлгЩ+3МлЩ§ИпЮЊ+6МлЃЌдђЙ§бѕЛЏЧтжаOдЊЫиЕФЛЏКЯМлгЩ-1МлНЕЕЭЮЊ-2МлЃЌЫљвджЄУїH2O2габѕЛЏадЃЌДэЮѓЃЛDЁЂгЩЂлжаШмвКБфРЖЃЌЩњГЩЕтЕЅжЪПЩжЊЃЌЗЂЩњбѕЛЏЛЙдЗДгІЃЌCrдЊЫиЕФЛЏКЯМлНЕЕЭЃЌIдЊЫиЕФЛЏКЯМлЩ§ИпЃЌгЩбѕЛЏМСЕФбѕЛЏадДѓгкбѕЛЏВњЮяЕФбѕЛЏадПЩжЊЃЌжЄУїбѕЛЏадЃКCr2O![]() >I2ЃЌе§ШЗЁЃ
>I2ЃЌе§ШЗЁЃ


 УћаЃПЮЬУЯЕСаД№АИ
УћаЃПЮЬУЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПьЂЃЈPH3ЃЉгжГЦСзЛЏЧтЃЌдкГЃЮТЯТЪЧвЛжжЮоЩЋгаДѓЫтГєЮЖЕФгаЖОЦјЬхЃЌЕчЪЏЦјЕФдгжЪжаГЃКЌгаСзЛЏЧтЁЃвдЯТЙигкPH3ЕФа№Ъіе§ШЗЕФЪЧ ( )
A. PH3ЗжзгжагаЮДГЩМќЕФЙТЖдЕчзг B. PH3ЪЧЗЧМЋадЗжзг
C. ЫќЕФЗжзгЙЙаЭЪЧЦНУцШ§НЧаЮ D. СздзгВЩгУsp2дгЛЏЗНЪН
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЗМЯуЫсРрЮяжЪFГЃгУзіЯуОЋЕФЕїЯуМСЁЃFЕФЁЊжжКЯГЩТЗЯпШчЯТЃК
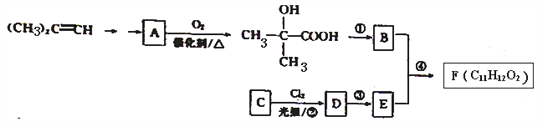
МКжЊЃКAФмЗЂЩњвјОЕЗДгІЁЃЛиД№ЯТСаЮЪЬтЃК
(1)(CH3)2=CH2ЕФЛЏбЇУћГЦЮЊ_________________ЃЌЩЯЪіЗДгІЂйЁЂЂкЁЂЂлЁЂЂмжаЪєгкШЁДњЗДгІЕФга_______________ЁЃ
(2)CЕФНсЙЙМђЪНЮЊ_________ЃЌDжаЭЈЙ§ЗДгІЂкв§ШЫЕФЙйФмЭХУћГЦЮЊ____________ЁЃ
(3)ЂйЕФЗДгІЬѕМўЪЧ__________________ЁЃ
(4)ЂмЕФЛЏбЇЗНГЬЪНЮЊ________________ЁЃ
(5)BЕФЭЌЗжвьЙЙЬхжаЃЌМШФмЗЂЩњвјОЕЗДгІгжФмЗЂЩњЫЎНтЗДгІЕФЙВга____жжЃЈВЛЬхвьЙЙЃЉЃЌЦфжаКЫДХЙВеёЧтЦзЯдЪОЮЊШ§зщЗхЃЌЧвЗхУцЛ§БШЮЊ1ЃК1ЃК4ЕФЪЧ________(ЬюНсЙЙМђЪН)ЁЃ
(6)аДГігУ(CH3)2C=CH2ЮЊдСЯ(ЮоЛњЪдМСШЮбЁ)жЦБИЛЏКЯЮяAЕФКЯГЩТЗЯпЃК____________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЯђВЛЭЌЕчНтжЪШмвКжаМгШыаТЮяжЪЪБШмвКЕФЕМЕчадФмЗЂЩњБфЛЏЃЌШчЯТЭМЫљЪОЪЧЦфЕчСї(I)ЫцаТЮяжЪМгШыСП(m)ЕФБфЛЏЧњЯпЁЃ
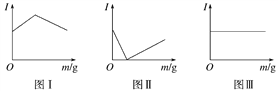
вдЯТ4ИіЕМЕчадЪЕбщЃЌЦфжагыЭМЂёЁЂЭМЂђЁЂЭМЂѓЖдгІвЛжТЕФбЁЯюЪЧ(ЁЁЁЁ)
ЂйBa(OH)2ШмвКжаЕЮШыH2SO4ШмвКжСЙ§СП
ЂкДзЫсШмвКжаЕЮШыNH3ЁЄH2OжСЙ§СП
ЂлГЮЧхЪЏЛвЫЎжаЭЈШыCO2жСЙ§СП
ЂмNH4ClШмвКжаж№НЅМгШыЪЪСПNaOHЙЬЬх
ЭМ бЁЯю | ЭМЂё | ЭМЂђ | ЭМЂѓ |
A | Ђй | Ђк | Ђл |
B | Ђм | ЂкЂл | Ђй |
C | Ђл | ЂйЂк | Ђм |
D | Ђк | ЂйЂл | Ђм |
A. A B. B C. C D. D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
A.ЖдгкгаЦјЬхВЮМгЕФЗДгІдіДѓбЙЧПФмЬсИпЛюЛЏЗжзгЕФХЈЖШ
B.Щ§ИпЮТЖШдіДѓСЫЛюЛЏЗжзгАйЗжЪ§
C.ДпЛЏМСФмЙЛИФБфЛЏбЇЗДгІЭООЖ
D.ОпгаНЯИпФмСПЕФЗДгІЮяЗжзгвЛЖЈФмЗЂЩњгааЇХізВ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉ3.01ЁС1024ИіOHЉЕФЮяжЪЕФСПЮЊ____ЃЌжЪСПЮЊ___ЃЌетаЉOHЉгыБъзМзДПіЯТ__L NH3ЕФЮяжЪЕФСПЯрЕШЃЌШчЙћетаЉOHЉРДзд2LЕФBa(OH)2ШмвКЃЌдђИУBa(OH)2ЕФЮяжЪЕФСПХЈЖШЮЊ__ЃЎ
ЃЈ2ЃЉЭЌЮТЭЌбЙЭЌЬхЛ§ЕФАБЦјЃЈNH3ЃЉКЭСђЛЏЧтЃЈH2SЃЉЦјЬхЕФжЪСПжЎБШЮЊ___ЃЌЫљКЌЕчзгЪ§жЎБШЮЊ__ЃЌЯрЭЌжЪСПЕФАБЦјКЭСђЛЏЧтЦјЬхЕФЗжзгЪ§жЎБШЮЊ______УмЖШжЎБШЮЊ______ЃЎ
ЃЈ3ЃЉБъПіЯТ8.96L ЕФCH4КЭCOЛьКЯЦјЬхЃЌЦфжЪСПЮЊ7.60gЃЌдђЦНОљФІЖћжЪСПЮЊ____________ЃЌCH4КЭCOЮяжЪЕФСПжЎБШЮЊ________________ЁЃ
ЃЈ4ЃЉвбжЊ100mLAl2(SO4)3ШмвКжаAl3+ ХЈЖШЮЊ0.6mol/LЃЌдђSO42-ЕФХЈЖШЮЊ______________ЃЌAl2(SO4)3ЕФЮяжЪЕФСПЮЊ_____________ЃЈВЛПМТЧAl3+ ЫЎНтЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏбЇЪЕбщЕФЛљБОВйзїЪЧЭъГЩЛЏбЇЪЕбщЕФЙиМќЃЌЯТСаЪЕбщВйзїе§ШЗЕФЪЧЃЈ ЃЉ
ЂйгУ50 mLСПЭВСПШЁ5.2 mLЯЁСђЫсЃЛ ЂкгУЗжвКТЉЖЗЗжРыБНКЭЫФТШЛЏЬМЕФЛьКЯЮяЃЛ
ЂлгУЭаХЬЬьЦНГЦСП117.7 gТШЛЏФЦОЇЬхЃЛ ЂмгУСПЭВСПШЁ23.10 mLфхЫЎЃЛ
ЂнгУеєЗЂУѓИпЮТзЦЩеЪЏЛвЪЏЃЛ ЂогУ250 mLШнСПЦПХфжЦ250 mL 0.2 molЁЄLЃ1ЕФNaOHШмвКЃЛ
A. ЂлЂо B. ЂкЂлЂмЂн C. ЂйЂкЂм D. ЂкЂнЂо
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩш![]() ЮЊАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаЫЕЗЈДэЮѓЕФЪЧ
ЮЊАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаЫЕЗЈДэЮѓЕФЪЧ
A. 1 molH2ЫљКЌЧтЦјЗжзгЪ§ЮЊ7![]()
B. 1 molAlгызуСПЕФЯЁбЮЫсШмвКЗДгІЩњГЩЧтЦј1.5 mol
C. дкБъзМзДПіЯТЃЌ0.5![]() ИіCl2ЫљеМЕФЬхЛ§дМЪЧ11.2L
ИіCl2ЫљеМЕФЬхЛ§дМЪЧ11.2L
D. дкБъзМзДПіЯТЃЌ22.4LH2OКЌгаЕФЗжзгЪ§ЮЊ![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГаЫШЄаЁзщЬНОПSO2ЦјЬхЛЙдFe3ЃЋЁЂI2ЃЌЫќУЧЪЙгУЕФвЉЦЗКЭзАжУШчЭМЫљЪОЃК
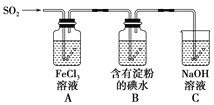
(1)AзАжУжаЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ_________________________________________ЁЃ
(2)BзАжУжаЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ_________________________________________ЁЃ
(3)ЯТСаЪЕбщЗНАИЪЪгУгкдкЪЕбщЪвжЦШЁЫљашSO2ЕФЪЧ________ЁЃ
AЃЎNa2SO3ШмвКгыHNO3 BЃЎNa2SO3ЙЬЬхгыХЈСђЫс
CЃЎЙЬЬхСђдкДПбѕжаШМЩе DЃЎЭгыШШХЈH2SO4
(4)зАжУCЕФзїгУЪЧ__________________________________________________ЁЃ
(5)ШєвЊДгAжаЫљЕУШмвКЬсШЁОЇЬхЃЌБиаыНјааЕФЪЕбщВйзїВНжшЃКеєЗЂЁЂРфШДНсОЇЁЂЙ§ТЫЁЂздШЛИЩдяЃЌдкетвЛЯЕСаВйзїжаУЛгагУЕНЕФвЧЦїга________(ЬюађКХ)ЁЃ
AЃЎеєЗЂУѓЁЁЁЁBЃЎЪЏУоЭјЁЁЁЁCЃЎТЉЖЗЁЁЁЁDЃЎЩеБ EЃЎВЃСЇАєЁЁЁЁFЃЎлслі
(6)дкЩЯЪізАжУжаЭЈШыЙ§СПЕФSO2ЃЌЮЊСЫбщжЄAжаSO2гыFe3ЃЋЗЂЩњСЫбѕЛЏЛЙдЗДгІЃЌЫћУЧШЁAжаЕФШмвКЃЌЗжГЩШ§ЗнЃЌВЂЩшМЦСЫШчЯТЪЕбщЃК
ЗНАИЂйЃКЭљЕквЛЗнЪдвКжаМгШыЫсадKMnO4ШмвКЃЌзЯКьЩЋЭЪШЅЁЃ
ЗНАИЂкЃКЭљЕкЖўЗнЪдвКжаМгШыKSCNШмвКЃЌВЛБфКьЃЌдйМгШыаТжЦЕФТШЫЎЃЌШмвКБфКьЁЃ
ЗНАИЂлЃКЭљЕкШ§ЗнЪдвКжаМгШыгУЯЁбЮЫсЫсЛЏЕФBaCl2ЃЌВњЩњАзЩЋГСЕэЁЃ
ЩЯЪіЗНАИВЛКЯРэЕФЪЧ________ЃЌдвђЪЧ____________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com