
下图为常温下用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1盐酸和20.00 mL 0.1000 mol·L-1醋酸的曲线。若以HA表示酸,下列判断和说法正确的是
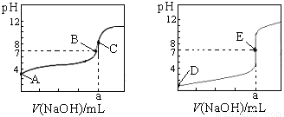
A.左图是滴定盐酸的曲线
B.E点时溶液中离子浓度为c(Na+) = c(A—)
C.B点时,反应消耗溶液体积:V(NaOH) <V(HA)
D.当0 mL< V(NaOH) < 20.00 mL时,对应溶液中各离子浓度大小顺序一定均为c(A-) >c(Na+)> c(H+) > c(OH-)
BC
【解析】
试题分析:A.盐酸是强酸,完全电离c(HCl)=0.1000mol/L,则c(H+)=0.1000mol/L,溶液的pH=1;醋酸是弱酸,部分电离,在溶液中存在电离平衡,c(H+)<c(CH3COOH)= 0.1000mol/L,所以溶液的pH>1.由于左图溶液在开始滴定时的pH>1,所以左图为滴定醋酸的图像,右图是滴定盐酸的图像,错误;B.由于右图是滴定盐酸的图像,在E点时溶液的pH=7,则酸碱恰好中和,c(H+) =c(OH-),根据电荷守恒可得c(Na+)+c(H+) =c(OH-) +c(A—)。所以溶液中离子浓度为c(Na+) = c(A—),正确;C.左图为NaOH溶液滴定醋酸的图像,由于产生的CH3COONa是强碱弱酸盐,若二者恰好完全反应,产生的盐的水溶液显碱性,在B点时,溶液显中性,说明滴加的碱的物质的量小于酸的物质的量,二者的浓度相等,所以反应消耗溶液体积:V(NaOH) <V(HA) ,正确;D.当0 mL< V(NaOH) < 20.00 mL时,在开始滴加不久,溶液中离子浓度大小关系是:c(A-) >c(Na+)> c(H+) > c(OH-);当溶液的pH=7时,离子浓度关系是:c(A-) =c(Na+)> c(H+) >=c(OH-);当溶液在B、C之间时,关系是:c(Na+)>c(A-) > c(OH-) > c(H+),因此不是总存在关系:c(A-) >c(Na+)> c(H+) > c(OH-),错误。
考点:考查酸碱中和滴定时溶液的pH和离子浓度大小比较的知识。
考点分析: 考点1:弱电解质的电离 考点2:盐类水解 试题属性

科目:高中化学 来源:2014-2015学年北京市石景山区高三一模理综化学试卷(解析版) 题型:选择题
下列解释物质用途或现象的反应方程式不正确的是
A.汽车尾气中发生的催化转化反应:2NO+2CO N2+2CO2
N2+2CO2
B.铝热反应用于焊接钢轨:2Al+Fe2O3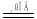 Al2O3+2Fe
Al2O3+2Fe
C.燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2 +O2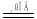 2CaSO3 +2CO2
2CaSO3 +2CO2
D.用Na2CO3溶液处理水垢中的不溶物CaSO4:CaSO4+CO32—===CaCO3+SO42—
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三下学期初考试理综化学试卷(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。

下列有关说法正确的是
A.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.步骤④的作用是达到富集溴的目的
C.过程②中MgCl2·6H2O加热脱水制得无水MgCl2
D.工业上电解熔融精盐的过程称为氯碱工业
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广西玉林市博白县高三下学期返校调研考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.滴入酚酞呈无色的溶液中:K+、Al3+、Cl-、CO32 -
B.澄清的溶液中:Na+、K+、MnO4—、AlO2—
C. =10-13 mol·L-1的溶液:Na+、[Ag(NH3)2]+、OH-、NO3-
=10-13 mol·L-1的溶液:Na+、[Ag(NH3)2]+、OH-、NO3-
D.c(I-)=0.1 mol·L-1的溶液中:Na+、H+、ClO-、SO42 -
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广西玉林市博白县高三下学期返校调研考试化学试卷(解析版) 题型:选择题
化学与生活息息相关.下列说法不正确的是
A.可用淀粉﹣KI试纸和食醋检验真假碘盐
B.用饱和氯化铵溶液可以清洗金属表面的锈迹
C.次氯酸钠溶液是生活中常用的消毒剂
D.经常食用含明矾的食品能中和过多的胃酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省湛江市高三高考测试(一)理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.22.4 L CH4中含有4 NA个C-H键
B.44g CO2含有2NA个氧原子
C.25 ℃,pH=1的硫酸溶液中含有的H+离子数为0.1NA
D.5.6g Fe与足量稀硝酸反应,转移的电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省汕头市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
氢氧燃料电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液。下列说法正确的是:
A.负极反应为:2H2+4OH- - 4e- = 4H2O
B.负极反应为:O2+2H2O+4e-= 4OH-
C.电池工作时溶液中的阴离子移向正极移动
D.电池工作时正极区pH升高,负极区pH下降
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省、广雅中学、佛山一中高三联考理综化学试卷(解析版) 题型:选择题
短周期元素甲、乙、丙、丁在周期表的相对位置如下表所示,其中乙为地壳含量最多的元素,则下列判断正确的是
甲 | 乙 | |
丙 | 丁 |
A.甲元素位于元素周期表中第2周期、第V族
B.甲、乙两元素能形成多种化合物
C.原子半径的大小:甲<乙
D.气态氢化物稳定性:丁>丙>乙
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省青岛市高三下学期一模考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.水的电离过程是吸热过程,升高温度,水的离子积增大、pH减小
B.根据CO2通入漂白粉水溶液中,溶液先变浑浊后澄清,推断SO2通入也有同样现象
C.向1 mL浓度均为0.05 mol·L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol·L-1的AgNO3溶液,振荡,沉淀呈黄色。结论:Ksp(AgCl)<Ksp(AgI)
D.将Fe(NO3)2晶体溶于稀硫酸,滴加KSCN溶液,通过观察溶液变红确定硝酸亚铁晶体已被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com