
【题目】合金是建造航空母舰的主体材料.
(1)航母升降机可由铝合金制造.
①铝元素在周期表中的位置为 ____________.
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为_________________.
(2)AlCl3也是重要的铝盐,无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备.
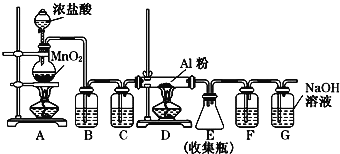
①装置A中发生反应的离子方程式为_____________________________________.
②装置B、C中盛放的试剂是B:__________ ,C:__________.
③装置G的作用是__________.
④无水AlCl3遇潮湿空气产生大量白雾的成分是__________.
【答案】 第三周期第ⅢA族 Al2O3+2NaOH=2NaAlO2+H2O MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 饱和食盐水 浓硫酸 吸收多余的Cl2,以防污染环境 盐酸
Mn2++Cl2↑+2H2O 饱和食盐水 浓硫酸 吸收多余的Cl2,以防污染环境 盐酸
【解析】(1)①根据Al的原子序数是13解答;
②氧化铝与NaOH溶液反应生成偏铝酸钠和水;
(2)①A中发生浓盐酸和二氧化锰的反应,生成氯化锰、氯气和水;
②无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,则装置B除去挥发的HCl,装置C干燥氯气;
③尾气中含氯气,需要尾气处理;
④氯化氢易形成盐酸小液滴而产生白雾。
(1)①Al的质子数是13,原子结构中有3个电子层,最外层电子数为3,位于第三周期第ⅢA族;
②氧化铝是两性氧化物,NaOH溶液处理Al2O3膜,反应生成偏铝酸钠和水,反应的方程式为Al2O3+2NaOH=2NaAlO2+H2O;
(2)①A中发生浓盐酸和二氧化锰的反应,生成氯化锰、氯气和水,离子反应方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
②无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,而生成的氯气中含有氯化氢和水蒸气,则装置B除去挥发的HCl,装置C干燥氯气,所以B中盛放饱和NaCl溶液,装置C中盛放浓硫酸;
③氯气有毒,需要尾气处理,则装置G的作用是吸收多余的Cl2,以防污染环境;
④无水AlCl3遇潮湿空气发生水解反应生成氯化氢,氯化氢易结合水蒸气形成盐酸小液滴而产生白雾,则产生大量白雾的成分是盐酸。


科目:高中化学 来源: 题型:
【题目】某同学在实验室中设计两个关于NO的探究实验。
(一)工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,探究NO和NH3能否反应。
(1)氨气的制备

①氨气的发生装置可以选择上图中的_____,反应的化学方程式______________________
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→__________(按气流方向,用小写字母表示)。
(2)将上述收集到的NH3加入少量催化剂,充入NO,充分混合,冷却到室温,观察到管中有少量水珠,说明NO和NH3能反应,则氧化剂和还原剂的物质的量之比为__________。
(二)探究一氧化氮能否被Na2O2完全吸收,设计了如下实验。装置如下(加热装置省略):

查阅资料所知:①2NO+Na2O22NaNO2
②酸性条件下,NO或NO2都能与KMnO4溶液反应生成NO3 -。
回答下列问题:
(1)仪器a名称:________________ 。
(2)B瓶内装的物质是:_______________ 。
(3)若NO能被Na2O2完全吸收,E装置中的现象为 ______________ 。
(4)三颈烧瓶A中反应的化学方程式为____________________________。
(5)C装置的作用是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(Bisphenol A dimethacrylate)是一种交联单体。合成F的一种路线如下:
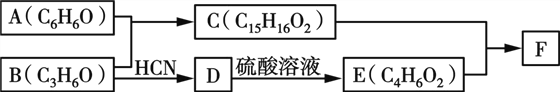
已知:
①![]() +HCN
+HCN![]()
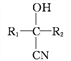
②B不能发生银镜反应。
③C能与FeCl3发生显色反应,核磁共振氢谱显示有4种不同化学环境的氢。
④E既能使溴水褪色又能使石蕊试液显红色。
⑤1 mol F最多可与4 mol NaOH反应。
回答下列问题:
(1)A与B反应的化学方程式为________________。
(2)B→D的反应类型为____,E的结构简式为________。
(3)F的结构简式为____________。
(4)C的同分异构体中含有萘环(![]() )结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的同分异构体共有____种(不考虑立体异构),其中核磁共振氢谱有8组峰的是____________(写出其中一种的结构简式)。
)结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的同分异构体共有____种(不考虑立体异构),其中核磁共振氢谱有8组峰的是____________(写出其中一种的结构简式)。
(5)A经如下步骤可合成环己烯甲酸:
A![]() G
G![]() H
H![]() I
I![]()
![]()
反应条件1为________;反应条件2为______;反应条件3所选择的试剂为____;I的结构简式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,mg下列物质在足量的氧气中充分燃烧后,产物与足量的过氧化钠充分反应,过氧化钠增加了ng,且n>m,符合此要求的物质是( )
①H2 ②HCHO ③CH4 ④HCOOCH3⑤CH3CHO
A. ①② B. ③⑤ C. ①②③④⑤ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是

A. a点对应的沉淀只有BaSO4
B. b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-==Al(OH)3↓+2BaSO4↓
C. c点溶液呈碱性
D. c点加入Ba(OH)2溶液的体积为200 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应属于取代反应的是( )
A. CH2=CH2+![]()
![]()
![]()
B. CH3CH=CH2+Cl2![]() CH2=CHCH2Cl+HCl
CH2=CHCH2Cl+HCl
C. 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D. CH3CH2Br+NaOH![]() CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是______________。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有 KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是___________。“滤液”中的溶质主要是________________。“调pH”中发生反应的化学方程式为_________________________。
(3)KIO3也可采用“电解法”制备,装置如图所示。

①写出电解时阴极的电极反应式_____________________________________。
②电解过程中通过阳离子交换膜的离子主要为_______________,其迁移方向是____________________。(“左到右”或“右到左”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com