
【题目】元素①~⑧在元素周期表中的位置如下,回答有关问题:
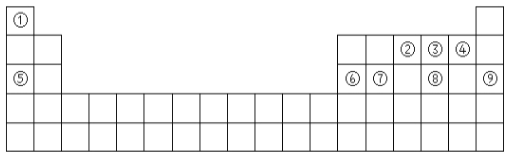
(1)表中能形成两性氢氧化物的元素是(填元素符号)______,最不活泼的元素的原子结构示意图为________。
(2)③号元素和⑧号元素的气态氢化物中,热稳定性较强的是(填化学式)________
(3)④号元素和⑥号元素的离子半径较大的是(填离子符号)_______
(4)上述元素中,金属性最强的元素与非金属最强的元素形成化合物的化学式______
(5)②的氢化物发生催化氧化的化学方程式为___________。
(6)写出⑤号元素的最高价氧化物对应的水化物和⑧号元素的最高价氧化物对应的水化物发生反应的离子方程式_______
【答案】Al 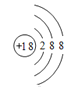 H2O F- NaF 4NH3+5O2
H2O F- NaF 4NH3+5O2![]() 4NO +6H2O H+ + OH- = H2O
4NO +6H2O H+ + OH- = H2O
【解析】
由元素在周期表中的位置可知,①为H、②为N、③为O、④为F、⑤为Na、⑥为Al、⑦为Si、⑧为S、⑨为Ar。结合元素周期律和元素及其化合物的性质分析解答。
由元素在周期表中的位置可知,①为H、②为N、③为O、④为F、⑤为Na、⑥为Al、⑦为Si、⑧为S、⑨为Ar。
(1)氢氧化铝属于两性氢氧化物,对应的元素为Al;稀有气体原子最外层为稳定结构,性质最不活泼,因此Ar的化学性质最不活泼,原子结构示意图为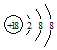 ,故答案为:Al;
,故答案为:Al;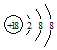 ;
;
(2)元素的非金属性越强,形成的氢化物越稳定,非金属性:O>S,故③号元素和⑧号元素的气态氢化物中,热稳定性较强的是H2O,故答案为:H2O;
(3)电子层数相同的微粒,核电荷数越大,半径越小,④号元素和⑥号元素都是2个电子层,因此离子半径较大的是F-,故答案为:F-;
(4)上述元素中,金属性最强的元素为钠,非金属最强的元素为氟,二者形成化合物的化学式为NaF,故答案为:NaF;
(5)元素②的氢化物为氨气,氨气催化氧化的化学方程式为4NH3+5O2![]() 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(6)元素⑤的最高价氧化物对应的水化物为氢氧化钠,属于强碱,⑧号元素的最高价氧化物对应的水化物为硫酸,属于强酸,二者反应的离子方程式为H+ + OH- = H2O,故答案为:H+ + OH- = H2O。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,由此判断表中所列M、N、P物质,其中可以成立的是

选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸 |
B | 铜 | 铁 | 稀盐酸 |
C | 银 | 锌 | 硝酸银溶液 |
D | 锌 | 铁 | 硝酸铁溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求。试回答以下问题:
(1)在仪器:a.分液漏斗 b.试剂瓶 c.集气瓶 d.滴定管 e.容量瓶 f.量筒 g.托盘天平中,标有“0”刻度的是_____________(填序号)。
(2)蒸发皿的使用:把滤液倒入蒸发皿中,再把蒸发皿放到铁架台的铁圈上。用酒精灯加热,同时用玻璃棒不断搅拌,以防止___________。当蒸发皿里的液体较少时,则应____________________,利用余热,使剩余溶剂挥发。
(3)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体。可供选择的液体试剂(固体试剂任选)有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。请回答下列问题:
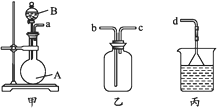
①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为____,制取该气体利用了B的性质有____、___________。
②通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为____;若在乙中收集氨气,气体流经装置的顺序是a→___→___→d(填接口代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl- 六种粒子。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是
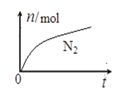
A. 该反应的还原剂是Cl-
B. 消耗1 mol还原剂,转移6 mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2.0 L的密闭容器内,物质D在T ℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是
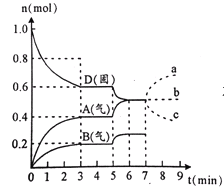
A. 从反应开始到第一次达到平衡时,A物质的平均反应速率为0.0667 mol/(L·min)
B. 该反应的化学方程式为2D(s) 2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B)
C. 已知:反应的H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度
D. 若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用废铅蓄电池的铅泥(含PbSO4、PbO和Pb等)可制备精细化工产品3PbO·PbSO4·H2O(三盐),主要制备流程如下。

请回答下列问题:
(1)铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为_____________。
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为_____________。
(2)将滤液Ⅰ、滤液Ⅲ合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为______________________。
(3)步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO。滤液Ⅱ中溶质的主要成分为______(填化学式)。
(4)步骤⑥合成三盐的化学方程式为______________________。
(5)步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于生物体内元素的叙述,正确的是( )
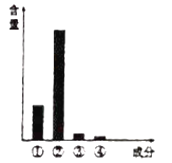
A. 各种元素在细胞与非生物界的含量差异不大
B. 细胞内含量最多的元素是C,因此C是生命的核心元素
C. 细胞内含有Fe、Cu、Mn、Zn、B、Mo等作用不重要的微量元素
D. 烘干的植物细胞中含量最多的元素是C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为 r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法中正确的是

A. X元素位于第ⅣA族
B. A能溶解于B中
C. A和C不可能发生氧化还原反应
D. B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两份等质量Na2O2和NaHCO3均匀混和物,向其中一份加入100mL盐酸,充分反应呈中性,放出气体经干燥后测得体积为2.24L(标准状况)。如将该气体通入另一混和物中充分反应后,气体体积变为2.016L(标准状况)。若混合物中NaHCO3的物质的量大于Na2O2。则:
(1)原混和物中Na2O2与NaHCO3的物质的量之比为__________________;
(2)加入盐酸的物质的量的浓度为_____________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com