
已知下面三个数据:①7.2×10 -4 ②2.6×10 -4 ③4.9×10 -10 分别是三种酸的电离平衡常数,若已知这三种酸可发生如下反应:NaCN+HNO 2 ==HCN+NaNO 2 NaNO 2 +HF==HCN+NaF NaNO 2 +HF==HNO 2 +NaF
由此可判断下列叙述中正确的是( )
A.HF的电离常数是① B.HNO2 的电离常数是①
C.HCN的电离常数是② D.HNO2 的电离常数是③
科目:高中化学 来源:2017届河南省高三上第三次周练化学试卷(解析版) 题型:填空题
Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒。
(1)电解NaCl溶液生成氯气的化学方程式为 。
(2)Cl2溶于H2O、NaOH溶液即获得氯水、漂白液。
①干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是 。
②25℃,Cl2与H2O、NaOH的反应如下:
反应Ⅰ | Cl2+H2O |
反应Ⅱ | Cl2+2OH- |
不直接使用氯水而使用漂白液做消毒剂的原因是 。
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+;ClO发生的电极反应式是 。
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如图所示:
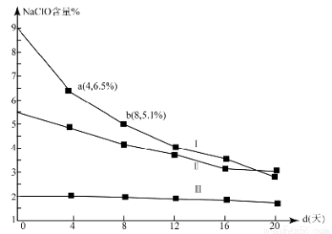
①分解速率v(Ⅰ) v(Ⅱ)(填“>”“<”或“=”),原因是 。
②NaClO分解的化学方程式是 。
③4d-8d,Ⅰ中v(NaClO)= mol/(L·d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一下期末化学试卷(解析版) 题型:推断题
实验中要测定某无色气体的成分,已知此气体可能由CO2、NH3、NO2、N2、NO中的一种或几种混合而成。将此无色气体进行以下实验:①先通过盛有浓硫酸的洗气瓶,发现气体减少一部分体积;②继续通过装有Na2O2固体的干燥管,发现从干燥管出来的气体颜色呈红棕色;③再继续将气体通入盛满水倒立于水槽中的试管内,最后气体完全被吸收,试管内充满液体。由此可判断:
(1)原气体中一定含有______________________,一定不含有_______________。
(2)写出②中发生反应的化学方程式_____________________________________。
(3)由最终结果可知原气体中__________和__________的体积比为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
一定条件下,可逆反应X(g)+3Y(g)=2Z(g)若X.Y.Z起始浓度分别为c1、c2、c3(均不为0),当达到平衡是X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
A.c1:c2=1:3
B.平衡时,Y 和Z的反应速率之比为3:2
C.X、Y的转化率不相等
D.c1的取值范围为0<c1<0.14mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
在甲酸的下列性质中,可以证明它是弱电解质的是( )
A.1mol/L的甲酸溶液中c(H+)约为0.01mol/L
B.甲酸与活泼金属反应生成氢气
C.10mL1mol/L的甲酸恰好与10mL1mol/L的NaOH溶液完全反应
D.在相同浓度下,甲酸的导电性比二元强酸溶液的弱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
在某恒温恒容的密闭容器内发生反应:2A(g)+B(g) C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是( )
C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是( )
A.再充入2mol A,平衡正移,A的转化率增大
B.如果升高温度,C的体积分数增大
C.如果增大压强,化学平衡一定向正反应方向移动,B的体积分数减小
D.再充入1mol C,C的物质的量浓度将增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第二次月考化学试卷(解析版) 题型:选择题
下列叙述中,不能用勒夏特列原理解释的是( )
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成SO3
C.加入催化剂有利于氨的合成
D.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上入学考试化学试卷(解析版) 题型:选择题
有以下四种物质:①标况下11.2LCO2 ②1g H2 ③1.204×1024个N2 ④4℃时18mLH2O,下列说法不正确的是( )
A.分子个数:③>④>①=② B.原子个数:③>④>①>②
C.体积:③>④>①=② D.质量:③>①>④>②
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上8月考试化学卷(解析版) 题型:填空题
在一个温度和体积不变的容器中,硫可以发生如下变化,其反应过程和能量关系如图1所示。(SO2(g)+1/2O2(g) SO3(g) △H=-98.45kJ·mol-1)
SO3(g) △H=-98.45kJ·mol-1)

(1)硫燃烧的热化学方程式为 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有 。
A.降低温度 B.充入He C.再充入1mol SO2(g)和1mol O2(g) D.使用催化剂
(3)恒温恒容时,图1中II到III反应放出的热量比1mol SO2和2mol O2充分反应放出的热量 (填
“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是 ;图中表示平衡混合物中SO3的含量最高的一段时间是 。(如t1~t2、t3~t4、t5~t6、t6~t7等)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com