
| A. | CH3CH2CH2CH2CH3 | B. | 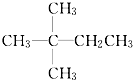 | C. | 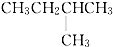 | D. | 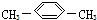 |
分析 1mol该烃燃烧需氧气179.2L(标准状况)即$\frac{179.2L}{22.4L/mol}$=8mol,可以确定烃的化学式,在光照的条件下与氯气反应能生成三种不同的一氯取代物,说明可取代3种不同的位置,以此进行判断.
解答 解:在光照的条件下与氯气反应能生成三种不同的一氯取代物,说明可取代3种不同的位置,
选项中各物质的一氯代物种类为: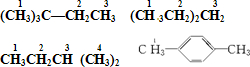 ,只有A、B选项符合要求,
,只有A、B选项符合要求,
而1mol该烃燃烧需氧气179.2L(标准状况)即$\frac{179.2L}{22.4L/mol}$=8mol,
A、B的分子式分别是C6H14和C5H12,
配平其燃烧方程式得:C6H14+9.5O2$\stackrel{点燃}{→}$6CO2+7H2O,C5H12+8O2$\stackrel{点燃}{→}$5CO2+6H2O,显然只有A符合,
故选A.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,试题较为综合,侧重于学生的分析能力和计算能力的考查,涉及有机化学基础、分子式、结构式、等价氢、燃烧方程式等知识,培养了学生灵活应用基础知识的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 1.5mol | B. | 3mol | C. | 4.5mol | D. | 6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:
为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形.RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中不正确的是( )
第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形.RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中不正确的是( )| A. | 分子中5个R-Cl键键能不都相同 | |
| B. | 键角(Cl-R-Cl)有90°、120、180°几种 | |
| C. | RCl5受热后会分解生成分子立体结构呈三角锥形的RCl3 | |
| D. | 每个原子都达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| B. | 过氧化钠的电子式: | |
| C. | 硫离子的结构示意图: | |
| D. | 苯的结构简式:C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
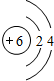 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com