
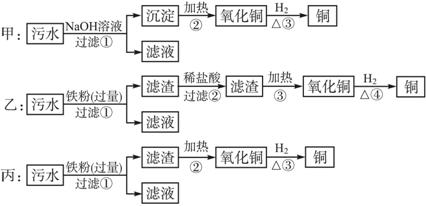
(1)以上实验方案能否得到铜(填“能”或“不能”):甲_______,乙_______,丙_______。?
(2)在制得铜的方案中会导致环境污染的一步操作是_______,其原因是________________。?
(3)在可制得铜的方案中,主要的离子方程式是________________________。?
解析:由于甲中加入NaOH溶液后Hg2+、Fe3+、Cu2+均沉淀下来,加热沉淀后所得固体物质应为CuO和Fe2O3的混合物(氧化汞加热分解产生汞,加热过程中挥发),用氢气还原后所得物质为铜和铁的混合物;乙中加入铁粉后因发生氧化还原反应产生铜和过量的铁,过滤,在滤渣中加入盐酸,此时铁溶解,再次过滤,加热汞挥发,最终得到铜单质;丙中加入铁粉后过滤,其中会混有铁粉,直接对滤渣加热,再用氢气还原导致制得的铜中混有铁粉。
答案:(1)不能 能 不能?
(2)③ 加热乙中操作②后的滤渣,此时汞蒸气将挥发进入空气中?
(3)Fe+2Fe3+=3Fe2+, Fe+Hg2+=Fe2++Hg, Fe+Cu2+=Fe2++Cu, Fe+2H+=Fe2++H2↑


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
太湖蓝藻暴发,造成无锡市自来水水源地水质的严重恶化。这次事件再次敲响了我国水危机的警钟。太湖流域某化工厂排放的污水中,常溶有某些对人体有害的物质,初步认为可能含有Fe3+、Ba2+、K+、OH-、Cl-、CO![]() 、SO
、SO![]() 。为了进一步确认,取样进行实验检测:
。为了进一步确认,取样进行实验检测:
①取污水仔细观察,呈无色、透明、均一状态。
②向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失。
③用pH试纸测定污水的pH,试纸显深蓝色。
(1)由此可知,该污水中肯定含有的离子是________________,肯定没有的离子是_____________,可能含有的离子是___________________。
(2)如何通过实验进一步确定溶液中可能存在的离子?
查看答案和解析>>
科目:高中化学 来源:2013年河南省开封市高考化学一模试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com