
已知热化学方程式:①C(金刚石,s)+O2(g)=CO2(g) △H1
②C(石墨,s)+O2(g)=CO2(g) △H2
③C(石墨,s)= C(金刚石,s) △H3=+1.9kJ/mol。下列说法正确的是
A.石墨转化成金刚石的反应是吸热反应 B.△H3=△H1-△H2
C.金刚石比石墨稳定 D.△H1>△H2
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源:2016-2017学年宁夏高二上学期开学考试化学试卷(解析版) 题型:填空题
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
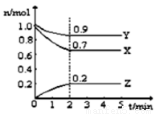
(1)由图中所给数据进行分析,该反应的化学方程式为 。
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)= 。
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填增大、减小或不变),混合气体密度比起始时 (填增大、减小或不变)。
(4)下列措施能加快反应速率的是 。
A.恒容时充入X B.及时分离出Z C.降低温度 D.选择高效的催化剂
(5)下列说法正确的是 。
A.升高温度可以改变化学反应的平衡状态
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.达到化学反应的平衡状态与时间长短无关
D.化学反应的平衡状态是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率减慢
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高一上开学考化学卷(解析版) 题型:选择题
关于0.1mol/LH2SO4溶液的叙述错误的是( )
A.1L该溶液中含有H2SO4的质量为9.8g
B.0.5L该溶液中氢离子的物质的量浓度为0.2mol/L
C.从1L该溶液中取出100mL,则取出溶液中H2SO4的物质的量浓度为0.01mol/L
D.取该溶液10mL,加水稀释至100mL后H2SO4的物质的量浓度为0.01mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高二上开学考化学卷(解析版) 题型:填空题
从NO3-、SO42-、H+、Cu2+、Ag+、Cl-中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解,写出符合下列要求的所有可能的电解质的化学式。
(1)两极分别放出H2和O2 。
(2)若阴极析出金属,阳极放出O2 。
(3)两极分别放出气体,且体积比为1:1 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高二上开学考化学卷(解析版) 题型:选择题
A、B、C、D为四种短周期元素,已知A、C同主族,B、D同周期;A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层。下列叙述正确的是
A. 原子序数:A>B>C>D B. 单质熔点:D>B,A>C
C. 原子半径:C>B>D>A D. 简单离子半径:C>A>D>B
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高二上开学考化学卷(解析版) 题型:选择题
据报道,挪威和荷兰正在开发一种新能源——盐能。当海水和淡水混合时,温度将升高0.1℃,世界所有入海口的这种能源相当于电力需求的20%,海水和淡水混合时,温度升高最可能的原因是
A.由于浓度差产生放热 B.发生了水分解反应
C.发生了盐分解反应 D.盐的溶解程度增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上入学考试化学试卷(解析版) 题型:选择题
某容积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:
A+3B 2C若维持温度和压强不变,当达到平衡时,容器容积为VL,其中C气体的体积占10%,下列推断正确的是( )
2C若维持温度和压强不变,当达到平衡时,容器容积为VL,其中C气体的体积占10%,下列推断正确的是( )
① 原混合气体的体积为1.2L ② 原混合气体的体积为1.1L
③ 反应达到平衡时气体A消耗掉0.05VL ④ 反应达到平衡时气体B消耗掉0.05VL
A.②③ B.②④ C.①③ D.①④
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三8月月考化学试卷(解析版) 题型:选择题
分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
A.冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物
B.HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸
C.漂白粉、福尔马林、冰水、王水、氯水均为混合物
D.Na2O,NaOH,Na2CO3,NaCl,Na2SO4,Na2O2都属于钠的含氧化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com