
���� ��ʼ����Cu+4H++2NO3-�TCu2++2NO2��+2H2O��Ũ�����淴Ӧ�Ľ��б�Ϊϡ���ᣬ��Ӧ�����ʱͭ��ϡ���ᷴӦ����NO�������ӷ�ӦΪ3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O��Cu��ʣ�࣬���������������ӣ���������������Һ�о���ǿ�����ԣ�����غ㷨���㣮
��� �⣺��1��Cu��Ũ���Ὺʼ��Ӧ�����ӷ���ʽΪCu+4H++2NO3-�TCu2++2NO2��+2H2O���۲쵽��ҺΪ��ɫ���к���ɫ�������ɣ�
�ʴ�Ϊ��Cu+4H++2NO3-�TCu2++2NO2��+2H2O����ҺΪ��ɫ���к���ɫ�������ɣ�
��2����ͭ��ʣ�࣬��Ӧ��Ҫ����ʱ�����ӷ���ʽΪ3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O���ʴ�Ϊ��3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O����
��3������Ӧֹͣ���ټ�������25%��ϡ���ᣬ��ʱͭƬ���������ݲ�����ԭ���Ǽ��������������ӣ���������������Һ�о���ǿ�����ԣ�
�ʴ�Ϊ�����������������ӣ���������������Һ�о���ǿ�����ԣ�
��4��12.8gCu�����ʵ���=$\frac{12.8g}{64g/mol}$=0.2mol����������ʵ���=$\frac{5.6L}{22.4L/mol}$=0.25mol�����ݵ�ԭ���غ㣬n��HNO3��=2n[Cu��NO3��2]+n��NO��NO2��=2��0.2mol+0.25mol=0.65mol���ʴ�Ϊ��0.65��
���� ���⿼��������ԭ��Ӧ�����㣬Ϊ��Ƶ���㣬���շ����ķ�Ӧ�����������Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע���غ㷨Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25g��������Ϊ68%��H2O2ˮ��Һ�к��е���ԭ����ĿΪNA | |
| B�� | ��״���£�11.2LCH3OH�к��еĹ��ۼ���ĿΪ2.5NA | |
| C�� | 42g�ɱ�ϩ��C3H6���ͻ����飨C3H6����ɵĻ�������к��е���ԭ����ĿΪ6NA | |
| D�� | 1L0.1mol•L-1NaHCO3��Һ��HCO${\;}_{3}^{-}$��${CO}_{3}^{2-}$��Ŀ֮��Ϊ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | ||
| C�� |  ��ϡ�����м����������Һ | D�� | 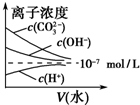 ϡ���մ���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 22.4LNO2����������Ϊ23NA | |
| B�� | 3.6gH2O�к��й��ۼ�������Ϊ0.2NA | |
| C�� | �����ɵ�����ͭŨ��Ϊ2mol/L����1L����Һ�к��е�Cu2+��Ϊ2N | |
| D�� | ����2molCu���뷴Ӧ������4molHNO3����ԭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ߴ���㷺�����������ά | |
| B�� | ��SO2ͨ�뵽BaCl2��Һ�п����ɰ�ɫ���� | |
| C�� | ��AlCl3��Һ�еμӰ�ˮ��������ɫ�������ټӹ�����NaHSO4��Һ��������ʧ | |
| D�� | CO��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��һ֧�Թ��з���һ���С��ͭƬ���ټ�������Ũ���ᣬȻ����Թ̶ܹ�������̨�ϣ���һС��պ��Ʒ����Һ����ֽ������е�����Ƥ���IJ������У������Թܿڣ��ڲ������ܿڴ�����һ��պ��Na2CO3��Һ���������Թܼ��ȣ��۲������Թ��е�Һ������ʱ��ֹͣ���ȣ�
��һ֧�Թ��з���һ���С��ͭƬ���ټ�������Ũ���ᣬȻ����Թ̶ܹ�������̨�ϣ���һС��պ��Ʒ����Һ����ֽ������е�����Ƥ���IJ������У������Թܿڣ��ڲ������ܿڴ�����һ��պ��Na2CO3��Һ���������Թܼ��ȣ��۲������Թ��е�Һ������ʱ��ֹͣ���ȣ� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com