
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HC1 | B. | 2CH3CH2OH+02$\stackrel{Cu、△}{→}$2CH3CH0+2H20 | ||
| C. | 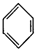 +HNO3$→_{50-60℃}^{浓硫酸}$ +HNO3$→_{50-60℃}^{浓硫酸}$ +H2O +H2O | D. | nCH2=CH2$\stackrel{一定条件}{→}$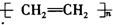 |
分析 A、甲烷光照条件下与氯气发生取代反应;
B、乙醇催化氧化反应生成乙醛;
C、苯与浓硝酸在浓硫酸催化下反应生成硝基苯;
D、乙烯发生加聚反应生成聚乙烯,聚乙烯中不含有碳碳双键.
解答 解:A、甲烷光照条件下与氯气发生取代反应生成多种卤代甲烷,其中之一是CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HC1,故A正确;
B、乙醇催化氧化反应生成乙醛,方程式为:2CH3CH2OH+02$\stackrel{Cu、△}{→}$2CH3CH0+2H20,故B正确;
C、苯与浓硝酸在浓硫酸催化下反应生成硝基苯,反应方程式为: +HNO3$→_{50-60℃}^{浓硫酸}$
+HNO3$→_{50-60℃}^{浓硫酸}$ +H2O,故C正确;
+H2O,故C正确;
D、乙烯发生加聚反应生成聚乙烯,聚乙烯中不含有碳碳双键,正确方程式应为: ,故D错误,故选D.
,故D错误,故选D.
点评 本题主要考查的是常见有机化学反应类型以及常见有机化合物的性质,难度不大,掌握烯烃的加聚反应原理是关键.


科目:高中化学 来源: 题型:多选题
| A. | .电池工作时,MnO2发生还原反应 | |
| B. | .电池负极的电极反应式为:2MnO2+H2O+2e-→Mn2O3+2OH- | |
| C. | .电池工作时,电路中每通过0.2mol电子,锌的质量理论上减少6.5g | |
| D. | 电池工作时,K+移向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
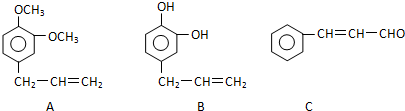
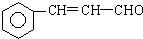 +5H2$\stackrel{一定条件下}{→}$
+5H2$\stackrel{一定条件下}{→}$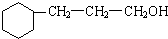 .
.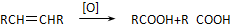 写出C在强氧化剂条件下生成的有机化合物的结构简式
写出C在强氧化剂条件下生成的有机化合物的结构简式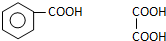 .
.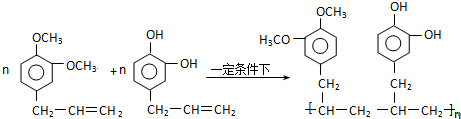 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溴苯中的溴(KI溶液) | B. | 溴乙烷中的乙醇(水) | ||
| C. | 苯中的苯酚(溴水) | D. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对泄露的苯酚用石灰水中和比用酒精冲洗掉的方法好 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升髙而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴人苯酚的水溶液后会放出二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解一定浓度的硫酸铜溶液,一段时间后,加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移电子数为0.4mol | |
| B. | 磷酸的电离方程式为:H3PO4=H++H2PO4- | |
| C. | 电镀时保持电流恒定,升温可知加快反应速率 | |
| D. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com