
| A. | 1mol任何气体的体积都约为22.4L | |
| B. | 22.4L水在标况下的质量为18g | |
| C. | 2L 1mol/L Na2CO3溶液中Na+浓度为4mol/L | |
| D. | 从1L NaCl溶液中取出100mL,其浓度与原1L溶液相同 |
分析 A.物质的量一定时,温度、压强影响气体的体积;
B.标况下水不是气体,22.4L水的物质的量远远大于1mol;
C.钠离子浓度为碳酸钠的2倍;
D.溶液是均一的,取出溶液、剩余溶液均与与原溶液浓度相等.
解答 解:A.物质的量一定时,温度、压强影响气体的体积,气体所处状态不确定,气体摩尔体积不一定是22.4L/mol,故A错误;
B.标况下水不是气体,22.4L水的物质的量远远大于1mol,质量远远大于18g,故B错误;
C.2L 1mol/L Na2CO3溶液中Na+浓度为2mol/L,故C错误;
D.溶液是均一的,从1L NaCl溶液中取出100mL,其浓度与原1L溶液相同,故D正确,
故选:D.
点评 本题考查气体摩尔体积、物质的量浓度、溶液性质等,比较基础,注意气体摩尔条件的使用条件与对象,根据PV=nRT理解温度、压强对气体摩尔体积的影响.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
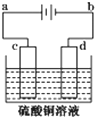 (1)电镀时,镀件与电源的负极连接.
(1)电镀时,镀件与电源的负极连接.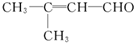 含氧官能团有醛基.
含氧官能团有醛基.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃、陶瓷、水泥 | B. | 塑料,合成纤维、橡胶 | ||
| C. | 青铜、碳素钢、硬铝 | D. | 玻璃钢、聚乙烯、超导陶瓷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、SO42-、CO32- | B. | Al3+、Na+、NO3- | C. | NH4+、OH-、SO32- | D. | Ag+、Cu2+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1700kJ | B. | 850kJ | C. | 425kJ | D. | 560kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
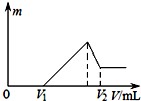
| A. | 向硫酸溶液中加入氢氧化钡溶液 | |
| B. | 向碳酸氢钠溶液中加入氯化钙 | |
| C. | 向硫酸、硫酸镁、硫酸铝的混合溶液中逐滴加入氢氧化钠溶液直至过量 | |
| D. | 向氯化铝溶液中加入过量氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
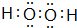 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上10月阶段测化学卷(解析版) 题型:选择题
在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体。在同温同压下,两容器内的气体一定具有相同的
A.原子数 B. 密度
C.分子数 D. 质子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com