
����Ŀ������10���ǻ���2����ϩ�ᣨHO![]() COOH�����10��HDA������Ȼ��ֻ�����ڷ������У�����Ҳ��Ϊ�����ᣬ�кܺõ�ɱ�����־����úͿ�����������Ĺ��ܡ��������һ���˹��ϳ�·��������£�
COOH�����10��HDA������Ȼ��ֻ�����ڷ������У�����Ҳ��Ϊ�����ᣬ�кܺõ�ɱ�����־����úͿ�����������Ĺ��ܡ��������һ���˹��ϳ�·��������£�
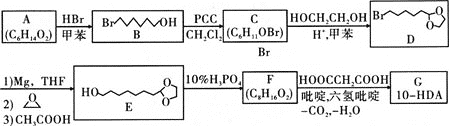
��֪��1mol A�����������Ʒ�Ӧ����1mol H2��C��F���ܷ���������Ӧ
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ________��A����B�ķ�Ӧ����Ϊ________��D�ķ���ʽΪ________��F�Ľṹ��ʽΪ________��
��2�����ý���ͭ������B����C���仯ѧ����ʽΪ________��
��3����C��D��E��F��ת�������ƶϴ���Ƶ�Ŀ����________��
��4��G��ͬ���칹������ͬʱ�������������Ĺ���________�֣������������칹����
�����뱥��̼��������Һ��Ӧ��������
�ں���Ԫ���ѽṹ������������CH2CH2CH2CH3��
���к˴Ź���������ʾΪ7������________��д�ṹ��ʽ����
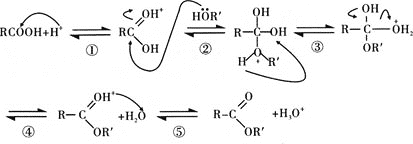
��5��G������ܷ���������Ӧ�������������Ӧ�����̿ɱ�ʾΪ����ͷ��ʾԭ�ӻ���ӵ�Ǩ�Ʒ���
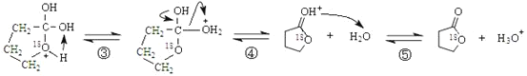
�ݴ����4���ǻ����������������4���ǻ����������ķ�Ӧ���̣�_______

���𰸡�1��6-������ ȡ����Ӧ C8H15O2Br HO(CH2)7CHO 2Br(CH2)5CH2OH+O2![]() 2Br(CH2)5CHO+2H2O ����ȩ�� 13
2Br(CH2)5CHO+2H2O ����ȩ�� 13 
��������
��1������1molA�����������Ʒ�Ӧ����1molH2����A�к���2�����ǻ�������B�Ľṹ��֪�����ǻ��ֱ������ˣ�����Ϊ��1��6-��������A����BΪ�ǻ�����ԭ��ȡ��������ȡ����Ӧ������D�Ľṹ��ʽ��֪��D�ķ���ʽΪ��C8H15O2Br��F�ܷ���������Ӧ����F�к���ȩ��������5Ԫ�����γ�ȩ������ṹ��ʽΪ��HO(CH2)7CHO��
��2�����ý���ͭ������B����C��B���ǻ�������Ϊȩ����
��3����C��D��E��F��ת��������γ�ȩ��������ȩ����
��4��G��ͬ���칹������ͬʱ�����������������뱥��̼��������Һ��Ӧ�������壬�ں���Ԫ���ѽṹ������������CH2CH2CH2CH3������ṹ����6Ԫ������2��ȡ������ͬһ��̼�Ϸֱ�����ԭ�Ӵ����ڡ��䡢��λ��3�֣��ֱ��ڲ�̼ͬԭ������7�֣����������Ȼ�����һ����3�֣���13�֡����к˴Ź���������ʾΪ7������ ��
��
��5�����������������Ӧ�����̣���֪4���ǻ����������������4���ǻ����������ķ�Ӧ���̡�
��1������1molA�����������Ʒ�Ӧ����1molH2����A�к���2�����ǻ�������B�Ľṹ��֪�����ǻ��ֱ������ˣ�����Ϊ��1��6-��������A����BΪ�ǻ�����ԭ��ȡ��������ȡ����Ӧ������D�Ľṹ��ʽ��֪��D�ķ���ʽΪ��C8H15O2Br��F�ܷ���������Ӧ����F�к���ȩ��������5Ԫ�����γ�ȩ������ṹ��ʽΪ��HO(CH2)7CHO���ʴ�Ϊ��1��6-��������ȡ����Ӧ��C8H15O2Br��HO(CH2)7CHO��
��2�����ý���ͭ������B����C��B���ǻ�������Ϊȩ�����仯ѧ����ʽΪ2Br(CH2)5CH2OH+O2 ![]() 2Br(CH2)5CHO+2H2O���ʴ�Ϊ��2Br(CH2)5CH2OH+O2
2Br(CH2)5CHO+2H2O���ʴ�Ϊ��2Br(CH2)5CH2OH+O2 ![]() 2Br(CH2)5CHO+2H2O��
2Br(CH2)5CHO+2H2O��
��3����C��D��E��F��ת��������γ�ȩ��������ȩ�����ʴ�Ϊ������ȩ����
��4��G��ͬ���칹������ͬʱ�����������������뱥��̼��������Һ��Ӧ�������壬�ں���Ԫ���ѽṹ������������CH2CH2CH2CH3������ṹ����6Ԫ������2��ȡ������ͬһ��̼�Ϸֱ�����ԭ�Ӵ����ڡ��䡢��λ��3�֣��ֱ��ڲ�̼ͬԭ������7�֣����������Ȼ�����һ����3�֣���13�֡����к˴Ź���������ʾΪ7������ ���ʴ�Ϊ��13��
���ʴ�Ϊ��13�� ��
��
��5�����������������Ӧ�����̣���֪4���ǻ����������������4���ǻ����������ķ�Ӧ����Ϊ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ķ�Ӧ·��������Ϣ��ա�
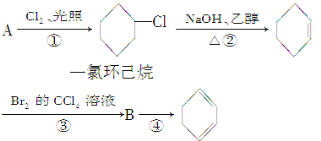
��1��A�Ľṹ��ʽ��______��������______��
��2�����ķ�Ӧ������______�����ķ�Ӧ������______��
��3����Ӧ���Ļ�ѧ����ʽ��__________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɣ���ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼװ����һ�������N��C��Si�ķǽ�����ǿ���Ƚϵ�ʵ���о�����ͬѧ�����û���Ӧ�Ĺ��ɣ�������ͼװ�������OԪ�صķǽ����Ա�Sǿ��ʵ���о����ش��������⣺

��1��ͼ��Dװ��������______��
��2��N��C��Si�ķǽ�������ǿ������˳���ǣ�______������������������ѡ����ͬѧ��Ƶ�ʵ�����õ����ʣ��Լ�AΪ______���Լ�CΪ______������ţ���
��ϡHNO3��Һ��ϡ������̼�����Na2SiO3��Һ��SiO2
��3������ͬѧ��Ƶ�ʵ�����õ��Լ�AΪ______���Լ�BΪ______���Լ�CΪ______����д���ƣ�
��д��C�з�����Ӧ�Ļ�ѧ����ʽ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ A(g)+3B(g)![]() 2C(g)+2D(g)���ڲ�ͬ����£�����������ĸ���Ӧ���ʣ��䷴Ӧ����������(����)
2C(g)+2D(g)���ڲ�ͬ����£�����������ĸ���Ӧ���ʣ��䷴Ӧ����������(����)
A. v(A)��0.15molL��1s��1B. v(B)��0.6molL��1s��1
C. v(C)��0.5molL��1s��1D. v(D)��0.4molL��1s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�������ѧ��������ƾ�跢�ֿ�ű��Чҩ�����أ�Ӯ����2015���ŵ��������ѧ���������صķ��������������ڶ�ű�����ߣ���Ϊ��ҽҩ�߳����ſ������Ⱥӣ������ص�һ�ֻ�ѧ�ϳɲ��ֹ����������£�
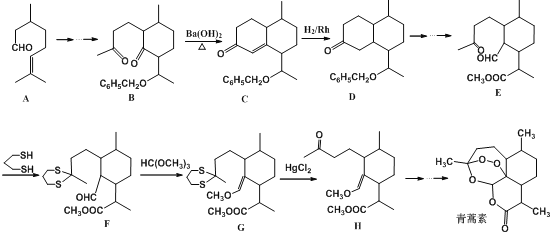
�������ػ����Ժϳ�ҩЧ��ǿ��ϵ��������
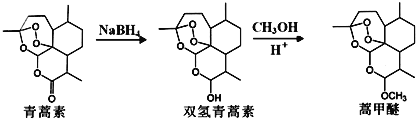
��1�������ط����к��еĺ����������У� ______ �� ______ ��������˫�������ط��ӽṹ�������ɸ���Ԫ������Ԫ����ɣ����к�����Ԫ����Ϊ ______ ������ѵĻ�ѧʽΪ ______ ��
��2����ӦB��C��ʵ���Ͽɿ����������У����η����ķ�Ӧ������ ______ ����ȥ��Ӧ��
��3���ϳ�·�������E��F��G��H��Ŀ���� ______ ��
��4��A��Sn-����ʯ�����£����칹Ϊ�����մ�![]() ���������մ������� ______ ������̼ԭ�ӣ��������ֲ�ͬԭ�ӻ�ԭ���ŵ�̼ԭ�ӳ�Ϊ����̼ԭ�ӣ��������մ���ͨ��������Ӧ����
���������մ������� ______ ������̼ԭ�ӣ��������ֲ�ͬԭ�ӻ�ԭ���ŵ�̼ԭ�ӳ�Ϊ����̼ԭ�ӣ��������մ���ͨ��������Ӧ����![]() ����д����ػ�ѧ��Ӧ����ʽ ______ �� ______ ��
����д����ػ�ѧ��Ӧ����ʽ ______ �� ______ ��
��5��д����A��Ϊͬ���칹�壬����������������ͬ���칹����ĿΪ ______ �֣������ǿռ��칹�������к˴Ź����������߸��壬�ҷ������Ϊ1��1��4��4��1��1��6���ǣ� ______ ������ṹ��ʽ��
�ٷ�����ֻ����һ����Ԫ����
����Ԫ����ֻ�ж���ȡ�������ڲ�ͬ��̼ԭ����
���ܹ�����������Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25�桢101kPa�£�1g�״�ȼ������CO2��Һ̬ˮʱ����22.68kJ�����б�ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽ��ȷ���ǣ�������
A. CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ��H=+725.8 kJ��mol��1
O2(g)=CO2(g)+2H2O(l) ��H=+725.8 kJ��mol��1
B. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ��H=-1452 kJ��mol��1
C. CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ��H=-725.8 kJ��mol��1
O2(g)=CO2(g)+2H2O(l) ��H=-725.8 kJ��mol��1
D. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ��H=+1 452 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(�Է�ĩ״����)�Ͱ�������������ͬ�������塣��֪��
��Sn (s����)��2HCl (aq)��SnCl2 (aq)��H2 (g)��DH1
��Sn (s����)��2HCl (aq)��SnCl2 (aq)��H2 (g)��DH2
��Sn (s����)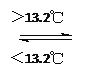 Sn (s����)��DH3����2.1 kJ/mol
Sn (s����)��DH3����2.1 kJ/mol
����˵����ȷ����( )
A. DH1��DH2
B. ���ڳ������Ի���״̬����
C. ����ת��Ϊ�����ķ�Ӧ�Ƿ��ȷ�Ӧ
D. ���������ڴ��ڵ���13.2 ���Ļ����У������лٻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ü״�����ϩ����ϩ��ϩ��ʱ�����¶�Ϊ400 ��ʱ������������ӦΪ2CH3OH![]() C2H4+2H2O��3CH3OH
C2H4+2H2O��3CH3OH![]() C3H6+3H2O������ӦΪ2CH3OH
C3H6+3H2O������ӦΪ2CH3OH![]() CH3OCH3+H2O����ϩ�ͱ�ϩ��ѡ����(ת���ļ״���������ϩ�ͱ�ϩ�İٷֱ�)����ϩ����ϩ�ı�ֵ(Cat.1��Cat.2�������ֵ����Ĵ���)��ͼ��ʾ������˵������ȷ����
CH3OCH3+H2O����ϩ�ͱ�ϩ��ѡ����(ת���ļ״���������ϩ�ͱ�ϩ�İٷֱ�)����ϩ����ϩ�ı�ֵ(Cat.1��Cat.2�������ֵ����Ĵ���)��ͼ��ʾ������˵������ȷ����
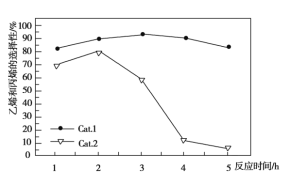
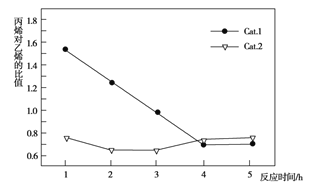
A. ʹ��Cat.2��Ӧ2Сʱ����ϩ�ͱ�ϩ��ѡ�����½�
B. ʹ��Cat.1��Ӧ3Сʱ�������ϩ����Ҫ����ϩ
C. ʹ��Cat.2��Ӧ3Сʱ�ڲ�����ϩ����Ҫ�DZ�ϩ
D. ʹ��Cat.1ʱ��ϩ�ͱ�ϩ��ѡ����һֱ����ʹ��Cat.2ʱ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ԭ���������ԭ�ӣ�������Ԥ��������������Ԫ��֮ĸ��ѧϰ���ʽṹ�����ʣ��ش��������⣺
(1)̫���е���Ҫ��ѧԪ�������_______��
(2)�⸺����H-��̬�����Ų�ʽΪ_______��
(3)���б仯��H-(g)=H(g)+e-���յ�����Ϊ73kJ/mol��H(g)=H+(g)+e-���յ�����Ϊ1311kJ/mol�����⸺����H-�ĵ�һ������Ϊ________��
(4)���ּ�����⻯��IJ����������±���ʾ��
�⻯�� | LiH | NaH | KH |
�ܶ�/g/cm3 | 0.78 | 1.43 | |
�ֽ��¶�/�� | 850 | 425 | 400 |
�ӻ�ѧ�ṹ�ĽǶȻش�˵�����ֽ��¶�LiH>NaH>KH___��
(5)ˮ��Һ����H3O+��H5O2+��H9O4+��������ʽ��H3O+�У�����ԭ�ӵ��ӻ�������___���뻭��H5O2+�Ľṹʽ��______�����ø�����������Һ̬ˮʱ��ˮ���ӱ���һ���µķ�ʽ���룬��ͼ��ʾд��������������ˮ���ܷ�Ӧ�����ӷ���ʽ_______��

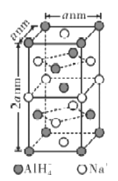
(6)�⻯����(NaAlH4)�ȸ����⻯������Ҫ���л���ԭ����NaAlH4�����ṹ��ͼ��ʾ��NaAlH4�����У���Na+�����ҵȾ��A1H4-��___�����谢��٤������ΪNA��������ܶ�Ϊ___g��cm-3��
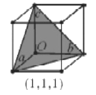
(7)�������������뾧����Խ��ߴ�ֱ�����ھ���ѧ�г�Ϊ��1��1��1)���档��ͼ��������������У�1��1��1)���湲��___����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com