
已知A、B、C均为短周期的元素,A、B同周期、A、C的最低价离子分别为A2﹣和C﹣,B2+和C﹣具有相同的电子层结构,下列说法正确的是( )
|
| A. | C元素的最高正价为+7价 |
|
| B. | 离子半径:A2﹣>C﹣>B2+ |
|
| C. | 对应气态氢化物的稳定性:A>C |
|
| D. | 还原性:A2﹣>C﹣ |
考点:
原子结构与元素周期律的关系.
专题:
元素周期律与元素周期表专题.
分析:
由A、C的最低价离子分别为A2﹣和C﹣,则A为ⅥA族元素,C为ⅦA族元素,B2+和C﹣具有相同的电子层结构,则B在C的下一周期,则B为Mg元素,C为F元素,A、B同周期,则A为S元素,
A.C为F元素,无正价;
B.具有相同核外电子结构的离子,核电荷数越大,半径越小;
C.非金属性越强的元素,其气态氢化物越稳定;
D.元素的非金属性越强,对应阴离子的还原性越弱.
解答:
解:由A、C的最低价离子分别为A2﹣和C﹣,则A为ⅥA族元素,C为ⅦA族元素,B2+和C﹣具有相同的电子层结构,则B在C的下一周期,则B为Mg元素,C为F元素,A、B同周期,则A为S元素,
A.C为F元素,无正价,最高价为0价,故A错误;
B.离子的电子层数越多,半径越大,具有相同核外电子结构的离子,核电荷数越大,半径越小,所以A2﹣>C﹣>B2+,故B正确;
C.C为F元素,A为S元素,F的非金属性大于S元素,所以HF的稳定性大于H2S,即对应气态氢化物的稳定性A<C,故C错误;
D.元素的非金属性越强,对应阴离子的还原性越弱,则有A2﹣>C﹣,故D正确.
故选BD.
点评:
本题考查原子结构与元素周期律的关系,为高频考点,侧重于学生的分析能力的考查,题目难度不大,本题的关键是根据原子结构特点正确推断元素的种类.


科目:高中化学 来源: 题型:
甲、乙、丙、丁是4种短周期元素,它们的原子序数依次增大,其中甲和丙、乙和丁分别是同主族元素,又知乙、丁两元素的原子核中质子数之和是甲、丙两元素的原子核中质子数之和的2倍,甲元素的一种核素核内无中子.
(1)丙、丁组成的常见化合物,其水溶液呈碱性,原因是
(用离子方程式表示);
写出两种均含甲、乙、丙、丁四种元素的化合物相互间发生反应,且生成气体的离子方程式 .
(2)丁的单质能跟丙的最高价氧化物的水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式 .
(3)甲、乙、丁可形成A、B两种微粒,它们均为﹣1价双原子阴离子,且A有18个电子,B有10个电子,则A与B反应的离子方程式为 .
(4)4.0g丁单质在足量的乙单质中完全燃烧放出37.0kJ热量,写出其热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要使用玻璃棒,其中玻璃棒作用相同的是( )
①过滤;②蒸发;③溶解;④向容量瓶中转移液体.
A. ①和④ B. ①和③ C. ③和④ D. ①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z 5种元素的叙述中,正确的是( )
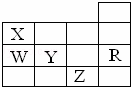
|
| A. | W、R元素单质分子内的都存在非极性键 |
|
| B. | X、Z元素都能形成双原子分子 |
|
| C. | 键能W﹣H<Y﹣H,键的极性Y﹣H>W﹣H |
|
| D. | 键长X﹣H<W﹣H,键能X﹣H<W﹣H |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
| a |
| ||||||||||||||||
| b | c | d | e |
| |||||||||||||
| f | g |
| |||||||||||||||
| h | i |
(1)请写出上述元素h的原子结构示意图 ;
(2)比较e、g两种元素的气态氢化物的稳定性大小 (写化学式,下同);e、g两种元素的气态氢化物熔、沸点较高的是 ,其原为 ;
(3)b2a2分子的电子式是 ,该分子中存在的σ键与π键的个数比为 ;
(4)c、d两种元素中第一电离能较大的是 (写元素符号),其原因是
;
(5)已知f的氢氧化物与水电离出的OH﹣可形成配位键,则生成的含有配位键的离子的结构式为 (标出配位键).
查看答案和解析>>
科目:高中化学 来源: 题型:
想一想:Ba(OH)2(固体)、CuSO4(固体)、纯醋酸(液态)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类( )
|
| A. | 75%的酒精溶液 | B. | 硝酸钠晶体 |
|
| C. | Fe(OH)3胶体 | D. | 豆浆 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2014秋•香坊区校级期中)从①渗析、②聚沉、③丁达尔效应 ④凝胶、⑤布朗运动、⑥电泳、中选出适当的序号填入下列每小题后面的空格中:
(1)用半透膜把制取的Fe(OH)3胶体中生成的氯化钠分离的方法叫做 .
(2)在肥皂水中透过强光,可见到光带,这种现象称为 .
(3)在Fe(OH)3胶体中加入(NH4)2SO4,产生红褐色沉淀,这种现象叫做 .
(4)在水泥厂和冶金厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染.这种做法应用的主要原理是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应的离子方程式书写正确的是( )
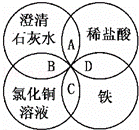
|
| A. | OH﹣+HCl═H2O+Cl﹣ | B. | Ca(OH)2+Cu2+═Ca2++Cu(OH)2 |
|
| C. | Fe+Cu2+═Cu+Fe2+ | D. | Fe+2H+═Fe3++H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com