
���� ��1�������к������������ǵ�����
��2�����������ˮʱ����������
��3��ʹ��ȼ�������������������
��4��ͬʱ���е����ס�������Ԫ���е����ֻ��������ϵķ��ϳ�Ϊ���Ϸʣ�
��5�����ڿ������������⣬���ڿ������ܹ��γɱ���Ĥ��
��� �⣺��1��������̼�����ÿ������������������棬�������ǵ�����
�ʴ�Ϊ��������
��2��������������ˮʱ���ȣ���ʹ�����¶Ƚ��ͣ�
�ʴ�Ϊ�����£�
��3��NH4H2PO4 ���ȷֽ���ڿ�ȼ������γ�һ�㲣��״�ĸ��Dz㣮�����ԭ���Ǹ���������
�ʴ�Ϊ������������
��4�����������к�����Ԫ�غ͵�Ԫ�أ����ڸ��Ϸʣ�
�ʴ�Ϊ��D��
��5�����ڿ������������⣬���ڿ������ܱ�����������һ�����ܶ���Ӳ�������ﱡĤ�������𱣻����ã��������ֹ���ʹ������ͬ��
�ʴ�Ϊ�����ڿ������������⣬���ڿ������ܱ�����������һ�����ܶ���Ӳ�������ﱡĤ�������𱣻����ã�
���� ������Ҫ�������ʵ����ʺ���;�����ʱҪ�������������ʵ����ʣ�Ȼ���ٸ������ʵ����ʷ�����з������жϣ��Ӷ�ȷ�����ʵ���;��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ�������ϣ�Ba2++2OH-+2H++SO42-�TBaSO4��+2H2O | |
| B�� | ��������������Һ��Ӧ��Fe+2Ag+�TFe2++2Ag | |
| C�� | �Ȼ�����Һ������İ�ˮ��Ӧ��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O | |
| D�� | ����ͨ���������������Һ�У�Cl2+2OH-�TCl-+ClO-+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ̼����狀�����������������Һ��Ӧ��NH4++OH-=NH3��+H2O | |
| B�� | ���Ȼ�����Һ��ͨ���������壺2Fe3++H2S=2Fe2++S��+2H+ | |
| C�� | ��ϡ�����������������Ӧ���Թܣ�Ag+2H++NO3-=Ag++NO2��+H2O | |
| D�� | ƫ��������Һ��ͨ������Ķ�����̼���壺2AlO2-+CO2+2H2O=2Al��OH��3��+CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 6 | 4 | x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ���е������仯��ͼ��ʾ�����H2=E1-E3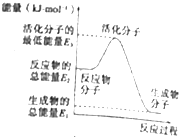 | |
| B�� | N2��ȼ����Ϊ180 kJ•mol-1 | |
| C�� | �ɷ�Ӧ��֪���¶�һ���������£���һ�����ܱ�������ͨ��1molN2��3molH2����Ӧ��ų�������ΪQ1kJ����Q1=92.4 | |
| D�� | ���Ĵ�������ӦΪ4NH3��g��+5O2��g��=4NO��g��+6H2O��g����H=-906 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H3PO2����ˮ�ĵ��뷽��ʽΪ��H3PO2?3H++PO23- | |
| B�� | H3PO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪ��H3PO2+3OH-=PO23-+3H2O | |
| C�� | ��H3PO2��Һ���뵽���Ը��������Һ�У�H3PO2�Ļ�ԭ����ΪH3PO4 | |
| D�� | �ö��Ե缫���NaH2PO2��Һ����������ӦʽΪ��H2PO2-4e-+2H2O=O2��+4H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Mg��HCO3��2��Һ�м�������� NaOH��Һ��Mg2++2HCO3-+4OH-=Mg��OH��2��+2CO32-��+2H2O | |
| B�� | FeBr2��Һ��ͨ������ʵ���Cl2��2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C�� | �����봿����Һ��Ӧ��2C6H5OH+CO32-=CO2��+H2O+2C6H5O- | |
| D�� | ��CuSO4��Һ�м���Na2O2��2Na2O2+2Cu2++2H2O=4Na++2Cu��OH��2��+O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��H+����c��OH-����c��CH3COO-����c��Na+�� | B�� | c��H+����c��OH-����c��Na+����c��CH3COO-�� | ||
| C�� | c��H+����c��CH3COO-����c��OH-����c��Na+�� | D�� | c��OH-����c��CH3COO-����c��H+����c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | m=aVd | B�� | a%=��cM/1 0d��% | C�� | c=1 000mVM | D�� | c=1 000daM |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com