
 ijѧ����0.1000mol/L KOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷֽ�Ϊ���¼�����
ijѧ����0.1000mol/L KOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷֽ�Ϊ���¼��������� ��1���к͵ζ��м�©��ϴ�ӡ���ϴ��װҺ���ζ��Ȳ�����
��2��ʵ�������ֿ��Ʋ����飬Ӧ�������ٲ��۲���ƿ����ɫ�仯������Һ��ɫ�仯�Ұ�����ڲ���ɫ����˵���ﵽ�ζ��յ㣻
��3������c�����⣩=$\frac{c��������V������}{V�����⣩}$���������ݹ�ϵʽHCl��KOH������������Ũ�ȣ�
��� �⣺�ζ��� 0�̶����Ϸ�������ͼ��֪�յ����Ϊ22.60mL���ʴ�Ϊ��22.60��
��1���к͵ζ����ռ�©��ϴ�ӡ���ϴ��װҺ��ȡ����Һ����ָʾ�����ζ���˳�����������ȷ��˳��ΪBEADCF���ʴ�Ϊ����B����E����A����D����C����F����
��2���ζ�ʱ����Ӧ���Ƽ�ʽ�ζ��ܵIJ����飬�Ա����Һ������٣�����ҡ����ƿ������Ӧ��ע����ƿ����Һ����ɫ�仯���ζ�ʱ����ƿ����Һ����ɫ����ɫ��dz���ұ��ְ�����ڲ���ɫ����˵���ﵽ�ζ��յ㣬
�ʴ�Ϊ����ʽ�ζ�����Ƥ�ܲ����鴦����ƿ����Һ����ɫ����ɫ��Ϊ�ۺ�ɫ�ұ��ְ���Ӳ���ɫ��
��3��������A������֮ǰ�������ô���Һ��ϴ��ƿ������Һ�����ʵ���ƫ�������ĵı�Һ���ƫ����c�����⣩=$\frac{c��������V������}{V�����⣩}$����֪c�����⣩ƫ��
����NaOH��Ħ������С��KOH������KOH�к���������NaOH������c������ƫ��V������ƫС���ʴ���Һ��Ũ��ƫС������ϴ�ζ��ܣ����±���Һ��ϡ�ͣ�V������ƫ����ô����Һ��Ũ��ƫ�ζ��������縩�ӹ۲�ζ�����Һ��̶ȣ���ôV�����⣩ƫ����ô����Һ��Ũ��ƫС��
���ı�KOH��Һ�����Ϊ22.60mL-4.60mL=18.00mL��
HCl��KOH
1 1
c��HCl����20.00mL 0.1000mol•L-1��18.00mL��
c��HCl��=$\frac{0.1000mol/L��18.00mL}{20.00mL}$=0.09000mol•L-1��pH=-log0.09=-��-2+2log3��=2-2��0.4771=1.0458��
�ʴ�Ϊ���٣��ڣ��٣��ڣ� 1.0458��1.046��
���� ���⿼���к͵ζ�����ȷ�ζ�ʵ���е����������ݴ������к͵ζ����������ǽ����Ĺؼ���ע������к͵�ʵ�ʣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Զ���֬���ȶ��ֲ�������� | |
| B�� | ��֬������ֱ�������������� | |
| C�� | ��֬��Ϊ��̬ | |
| D�� | ��Щ֬�������������ģ���������ȴ���ܺϳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������㷺����ҽҩ��ʳƷ��Ⱦ�ϡ�����������������ʵ�����Ʊ��������һ�ַ�������Ӧԭ�����£�
������㷺����ҽҩ��ʳƷ��Ⱦ�ϡ�����������������ʵ�����Ʊ��������һ�ַ�������Ӧԭ�����£� +2KMnO4$\stackrel{��}{��}$
+2KMnO4$\stackrel{��}{��}$ +2MnO2��+KOH+H2O
+2MnO2��+KOH+H2O +HCl��
+HCl��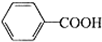 ��+KCl
��+KCl| ���� | ��Է������� | ��״ | �۵�/�� | �ܽ�� | |
| ˮ | �Ҵ� | ||||
| �ױ� | 92 | ��ɫҺ����ȼ�ӷ� | -96 | ���� | ���� |
| ������ | 122 | ��ɫƬ״����״���� | 122.4 ��100�������� | 25��0.35g 80��2.7g | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵�����������ӣ�����A��B��A��D�����ڱ���λ�����ڣ�Aԭ�Ӻ���������δ�ɶԵ��ӣ�BԪ�صĵ�һ�����ܱ�ͬ������������Ԫ�ض���Cԭ����ͬ����ԭ���а뾶���ϡ��������⣩��E��Cλ�ڲ�ͬ���ڣ�Eԭ�Ӻ���������������C��ͬ�����������Ӿ������������������Ϣ���ش��������⣺������ʱA��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ��
��֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵�����������ӣ�����A��B��A��D�����ڱ���λ�����ڣ�Aԭ�Ӻ���������δ�ɶԵ��ӣ�BԪ�صĵ�һ�����ܱ�ͬ������������Ԫ�ض���Cԭ����ͬ����ԭ���а뾶���ϡ��������⣩��E��Cλ�ڲ�ͬ���ڣ�Eԭ�Ӻ���������������C��ͬ�����������Ӿ������������������Ϣ���ش��������⣺������ʱA��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| X | Y | Z | M | R | Q | |
| ԭ�Ӱ뾶/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| ��Ҫ���ϼ� | -4��+4 | -2 | -1��+7 | +3 | ||
���� | �����Ӻ������� | �����뵼����� | ��ɫ��Ӧ�ʻ�ɫ |
 ��R����Ȼ������������Ϊ35��37�����ֺ��أ�����֮��Ĺ�ϵ��Ϊͬλ�أ�
��R����Ȼ������������Ϊ35��37�����ֺ��أ�����֮��Ĺ�ϵ��Ϊͬλ�أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol������1mol��������ȫ��Ӧ��Ҫ����26kJ������ | |
| B�� | 1������Ӻ�1���������ȫ��Ӧ��Ҫ����52kJ������ | |
| C�� | 1mol H2��g����1mol I2��g����ȫ��Ӧ����2mol��HI��g��������52kJ������ | |
| D�� | 1mol H2��g����1mol I2��g����ȫ��Ӧ�ų�26kJ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com