
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
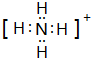 (用元素符号表示).
(用元素符号表示).分析 短周期元素中,T元素原子M层上有2对成对电子,则M层电子排布为3s23p4,故T为S元素;X元素原子最外层电子数是次外层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故X为C元素;常温下Y单质为双原子分子,其氢化物水溶液呈碱性,可知Y是N元素;元素Z最高正价是+7价,则Z是Cl,以此解答该题.
解答 解:短周期元素中,T元素原子M层上有2对成对电子,则M层电子排布为3s23p4,故T为S元素;X元素原子最外层电子数是次外层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故X为C元素;常温下Y单质为双原子分子,其氢化物水溶液呈碱性,可知Y是N元素;元素Z最高正价是+7价,则Z是Cl.
(1)元素T的最外层电子排布为3s23p4,原子最外层有6个电子,则有6种不同运动状态的电子,元素C的一种同位素可测定文物年代,该同位素含有8个中子,则中子数为6+8=14,这种同位素的符号是14C,
故答案为:6;14C;
(2)元素Y与氢元素形成一种离子NH4+,该微粒的电子式为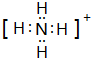 ,
,
故答案为: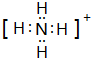 ;
;
(3)S和Cl位于周期表相同周期,Cl元素非金属性较强,可根据氢化物的稳定性、最高价含氧酸的酸性强弱、单质之间相互置换等进行判断,单质都能与氢氧化钠反应、单质状态、原子最外层电子数,都不能用于比较非金属性,
故答案为:Cl;bef;
(4)氯元素有多种常见含氧酸,氯元素化合价越高,含氧酸的酸性越强,常见含氧酸由强到弱的顺序是:HClO4>HClO3>HClO,
故答案为:HClO4>HClO3>HClO.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意掌握金属性、非金属性强弱比较实验事实,难度不大.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:填空题
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | |||||||
| 3 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ①③⑤ | C. | ②④ | D. | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 银氨溶液 | B. | 金属钠 | ||
| C. | FeCl3溶液 | D. | 新制的Cu(OH)2碱性悬浊液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com