
下列有关实验装置进行的相应实验,能达到实验目的的是
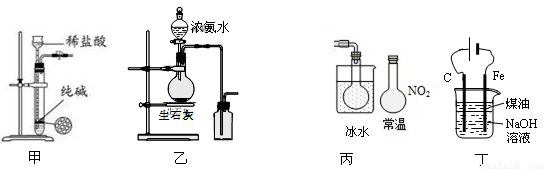
A.用图甲所示装置控制制取少量纯净的CO2气体
B.用图乙所示装置制取并收集氨气
C.用图丙所示装置可以说明反应2NO2(g) N2O4(g)是放热反应
N2O4(g)是放热反应
D.用图丁所示装置可制备Fe(OH)2并能较长时间观察其颜色
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年江苏省南通、扬州、连云港高三第二次调研测试化学试卷(解析版) 题型:选择题
下列说法正确的是
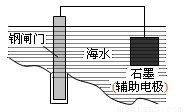
A.用上图所示方法可保护钢闸门不被腐蚀
B.SiO2(s)+2C(s)=Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0
C.常温下,NH4Cl溶液加水稀释,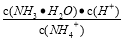 增大
增大
D.C(s)+H2O(g)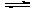 CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动
CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
(14分)Ⅰ.(1)下图为1molNO2(g)和1molCO(g)反应生成NO(g)和 CO2(g)过程中的能量变化示意图。
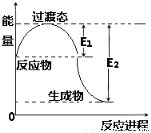
已知E1=134KJ/mol,E2=368KJ/mol(E1、E2为反应的活化能)。若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是 (填“增大”、“减小”或“不变”)。写出该反应的热化学方程式 。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H ____ 0
A.大于 B.小于 C.等于 D.大于或小于都可
Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。
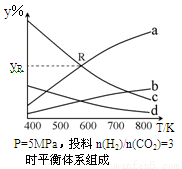
完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大
B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变
D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2
C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省毕业生复习统一检测理综化学试卷(解析版) 题型:选择题
250C时,物质的量浓度相等的NaHCO3, CH3COONa混合溶液中,下列有关说法或粒子浓度关系正确的是(Ka表示CH3COOH的电离平衡常数)
A.pH可能等于7
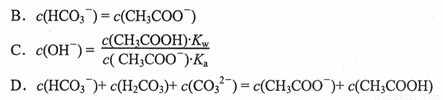
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市七校高三4月联考化学试卷(解析版) 题型:简答题
(共15分)不饱和酯类化合物在药物、涂料等领域应用广泛。
(1)下列关于化合物I的说法,正确的是
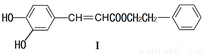
A.可能发生酯化反应和银镜反应
B.1mol化合物I最多与2molNaOH反应
C.与FeCl3溶液能显紫色
D.能与溴发生取代和加成反应
(2)下面反应是一种由烯烃直接制备不饱和酯的新方法
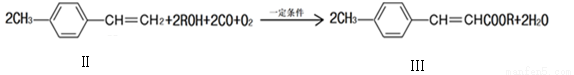
①化合物II的分子式为 。
②1mol化合物II能与 molH2恰好反应生成饱和烃类化合物。
③化合物Ⅲ与足量的NaOH溶液共热的化学方程式为 ;反应类型:
(3)3﹣对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
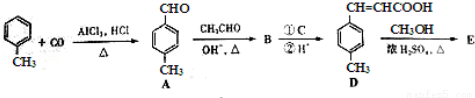
已知:HCHO+CH3CHO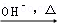 CH2=CHCHO+H2O
CH2=CHCHO+H2O
①A中官能团的名称为 。D中含氧官能团的名称为 。
②E的结构简式为 。
③试剂C可选用下列中的
a、溴水 b、银氨溶液
c、酸性KMnO4溶液 d、新制Cu(OH)2悬浊液
④B在一定条件下可以生成高聚物F,该反应的化学方程式为 _________ 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河西区高三下学期总复习质量调查(二)化学试卷(解析版) 题型:填空题
(14分)X、Y、Z、M四种短周期元素的原子半径依次减小。甲、乙、丙是由它们形成的三种常见分子;甲是人体必需的基本营养物质之一,约占人体体重的2/3;乙是日常生活的基础能源,其中含元素Y的质量分数为75%;丙是具有强氧化性的弱酸。丁为丙的钠盐,常用于漂白或消毒。戊与甲的组成元素相同,其分子具有18电子。请按要求回答下列问题:
(1)元素X、Y的最高价氧化物的水化物的酸性由强到弱为(填化学式)_______;丁的电子式为___________;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)______________、______________。
(2)元素E、F与X同周期。
①常温下E的单质与甲反应缓慢,加热至沸反应迅速,滴加酚酞试液,溶液变红色;此反应的化学方程式为 。
②F的单质粉末加油漆后即得“银粉漆”,在汽车漆家族中有重要地位。写出保存“银粉”时的注意事项:________________、__________________等。
(3)向盛有一定浓度戊溶液的烧杯中逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中可依次观察到的现象:
a.浅绿色溶液变成黄色
b.有少量气泡产生,片刻后反应变得更剧烈,并放出较多热量
c.继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀
①现象a中反应的离子方程式:________________________________________;
②现象b中反应剧烈的化学方程式:____________________________________;
③解释现象c:________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
(14分)钠及其化合物具有广泛的用途。
(1)工业上制备金属钠的常用方法是____________。试写出制备金属钠的化学方程式 。金属钠可用于 (写出Na在熔点低方面的一种用途)。
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示:

①正极的电极反应式为___________,电池工作时物质A可循环使用,A物质的化学式为_____________。
②请写出检验Na2CO3中钠元素的方法 。
(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 11.6 | 10.3 | 11.1 |
上述盐溶液的阴离子中,结合H+能力最强的是 ,根据表中数据,浓度均为0.01 mol·L-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是_______(填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当300 mL 1 mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为________________________。
②已知几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时,________(填离子符号)先沉淀,Ksp[Fe(OH)2]______Ksp[Mg(OH)2](填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三下学期第二次月考化学试卷(解析版) 题型:选择题
向下图所示的装置中缓慢地通入气体X,若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色。X和Y可能是
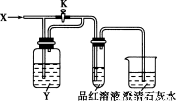
A | B | C | D | |
X | SO2 | C12 | HCl | NO2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
某未知溶液可能含Na+、NH4+、Fe2+、I-、Cl-、CO32-、SO32-。将该溶液加少量新制氯水,溶液变黄色。再向上述反应后溶液中加入BaCl2溶液或淀粉溶液,均无明显现象。下列推断合理的是
A.一定存在Fe2+、Na+、Cl- B.一定不存在I-、SO32-
C.一定呈碱性 D.一定存在NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com