
| N |
| NA |
| N |
| NA |
| N |
| NA |
| ||
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 2 |
| N |
| NA |
| ||
| 6.02×1023/mol |


科目:高中化学 来源: 题型:
| A、NaClO、NaClO2、KClO3、NaClO4中Cl的化合价依次升高 |
| B、C与CuO高温共热,C的氧化产物只能是CO2 |
| C、H2SO4由分子构成,溶于水离解成H+和SO42- |
| D、Al与Fe2O3高温反应生成Al2O3与Fe,属于置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 试剂 | 钠 | 酸性高锰酸钾溶液 | NaHCO3溶液 |
| 现象 | 放出气体 | 褪色 | 不反应 |
| A、CH2═CH-COOH |
| B、CH2═CHCH3 |
| C、CH3COOCH2CH3 |
| D、CH2═CHCH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图,在密闭容器中反应:C(s)+H2O(g)?CO(g)+H2(g) (吸热反应)达到平衡后,由于条件的改变而引起正、逆反应速率的变化,及平衡移动状况,则改变的条件是( )
如图,在密闭容器中反应:C(s)+H2O(g)?CO(g)+H2(g) (吸热反应)达到平衡后,由于条件的改变而引起正、逆反应速率的变化,及平衡移动状况,则改变的条件是( )| A、增加CO浓度 | B、增大压强 |
| C、升高温度 | D、增加水蒸气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
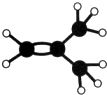 如图是某烃A分子的球棍模型.回答下列问题:
如图是某烃A分子的球棍模型.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com