
| A£® | lmolµÄNa2CO3ČÜÓŚŃĪĖįŠĪ³É»ģŗĻČÜŅŗ1L£¬³£ĪĀĻĀŌŚpH=4Ź±£¬c£ØCO32-£©+c£ØHCO3-£©+c£ØH2CO3£©=0£®lmol/L | |
| B£® | ±ź×¼×“æöĻĀ£¬2.24 LŅ»ĀČ¼×ĶéÖŠŗ¬ÓŠĒāŌ×ÓŹżÄæĪŖ0.3NA | |
| C£® | µČĪļÖŹµÄĮæµÄO2ŗĶCO2Ėłŗ¬ŃõŌ×ÓŹż¾łĪŖ2NA | |
| D£® | 6.8 gČŪČŚµÄKHSO4ÖŠŗ¬ÓŠ0.1 NAøöŃōĄė×Ó |
·ÖĪö A£®lmolµÄNa2CO3ČÜÓŚŃĪĖįŠĪ³É»ģČÜŅŗ1L£¬ČÜŅŗÖŠĢ¼ŌŖĖŲø÷ÖÖ“ęŌŚŠĪŹ½×ÜÅضČĪŖ1mol/L£»
B£®±ź×¼×“æöĻĀ£¬2.24 LŅ»ĀČ¼×ĶéĘųĢåĪļÖŹµÄĮæn=$\frac{2.24L}{22.4L/mol}$=0.1mol£¬Ņ»ĀČ¼×ĶéÖŠŗ¬ČżøöĒāŌ×Ó£»
C£®O2ŗĶCO2·Ö×ÓÖŠĖłŗ¬ŃõŌ×ÓŹż¶¼ŹĒ2øö£¬ĖłŅŌµČĪļÖŹµÄĮæµÄO2ŗĶCO2£¬ŗ¬ŃõŌ×ÓŹżĻąĶ¬£¬µ«²»Ņ»¶ØŹĒ2mol£»
D£®øł¾ŻČŪČŚµÄKHSO4Ö»ÄܵēĄėĪŖK+ŗĶHSO4-Ą“·ÖĪö£®
½ā“š ½ā£ŗA£®lmolµÄNa2CO3ČÜÓŚŃĪĖįŠĪ³É»ģČÜŅŗ1L£¬ČÜŅŗÖŠĢ¼ŌŖĖŲø÷ÖÖ“ęŌŚŠĪŹ½×ÜÅضČĪŖ1mol/L£¬³£ĪĀĻĀŌŚpH=4Ź±£¬c£ØCO32-£©+c£ØHCO3-£©+c£ØH2CO3£©=lmol/L£¬¹ŹA“ķĪó£»
B£®±ź×¼×“æöĻĀ£¬2.24 LŅ»ĀČ¼×ĶéĘųĢåĪļÖŹµÄĮæn=$\frac{2.24L}{22.4L/mol}$=0.1mol£¬2.24 LŅ»ĀČ¼×ĶéÖŠŗ¬ÓŠĒāŌ×ÓŹżÄæĪŖ0.3NA £¬¹ŹBÕżČ·£»
C£®µČĪļÖŹµÄĮæµÄO2ŗĶCO2£¬ŗ¬ŃõŌ×ÓŹżĻąĶ¬£¬µ«²»Ņ»¶ØŹĒ2mol£¬¹ŹC“ķĪó£»
D.6.8gČŪČŚµÄKHSO4µÄĪļÖŹµÄĮæn=$\frac{m}{M}$=0.05mol£¬¶ųČŪČŚµÄKHSO4Ö»ÄܵēĄėĪŖK+ŗĶHSO4-£¬¹Ź0.05molČŪČŚµÄKHSO4ŗ¬0.05molŃōĄė×Ó£¬øöŹżĪŖ0.05NAøö£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÓŠ¹Ų¼ĘĖć£¬ĘųĢåĦ¶ūĢå»żÓ¦ÓĆĢõ¼ž·ÖĪö£¬ÕĘĪÕ¹«Ź½µÄŹ¹ÓĆŗĶĪļÖŹµÄ½į¹¹”¢×“Ģ¬ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 øßÖŠ±ŲĖ¢ĢāĻµĮŠ“š°ø
øßÖŠ±ŲĖ¢ĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃĪĖį | B£® | ĢśĘ¬ | C£® | KSCNČÜŅŗ | D£® | ŹÆČļČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ó | B£® | Š” | ||
| C£® | ĻąĶ¬ | D£® | æÉÄܱä“óŅ²æÉÄܱ䊔 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
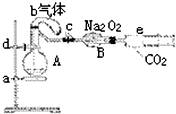 ČēĶ¼ĖłŹ¾×°ÖĆÖŠ£¬aŹĒŹ¢ÓŠ±źæöĻĀ224mLæÕĘų£ØŃõĘųÕ¼Īå·ÖÖ®Ņ»£©ŗĶ10mL 1.2mol/LĻõĖįµÄÉÕĘ棬bŹĒĪ“³äĘų£ØŹµŃéæŖŹ¼Ē°ÄŚ²æƻӊĘųĢ壩װӊ0.384gĶ·ŪµÄĘųĒņ£¬cŹĒ¼Š½ōĮĖµÄµÆ»É¼Š£¬dÖŠŹ¢ÓŠ×ćĮæµÄ¹żŃõ»ÆÄĘ£¬eŹĒ³äÓŠ¶žŃõ»ÆĢ¼µÄ×¢ÉäĘ÷£®ÕūĢ××°ÖĆ¾¹żĘųĆÜŠŌ¼ģ²éŅŃŗĻøń£®
ČēĶ¼ĖłŹ¾×°ÖĆÖŠ£¬aŹĒŹ¢ÓŠ±źæöĻĀ224mLæÕĘų£ØŃõĘųÕ¼Īå·ÖÖ®Ņ»£©ŗĶ10mL 1.2mol/LĻõĖįµÄÉÕĘ棬bŹĒĪ“³äĘų£ØŹµŃéæŖŹ¼Ē°ÄŚ²æƻӊĘųĢ壩װӊ0.384gĶ·ŪµÄĘųĒņ£¬cŹĒ¼Š½ōĮĖµÄµÆ»É¼Š£¬dÖŠŹ¢ÓŠ×ćĮæµÄ¹żŃõ»ÆÄĘ£¬eŹĒ³äÓŠ¶žŃõ»ÆĢ¼µÄ×¢ÉäĘ÷£®ÕūĢ××°ÖĆ¾¹żĘųĆÜŠŌ¼ģ²éŅŃŗĻøń£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē½āČŪČŚµÄAl2O3æÉŅŌÖĘµĆ½šŹōĀĮŗĶŃõĘų£¬øĆ·“Ó¦ŹĒŅ»øö·Å³öÄÜĮæµÄ·“Ó¦ | |
| B£® | Ė®·Ö½ā²śÉśĒāĘųŗĶŃõĘųŹ±·Å³öÄÜĮæ | |
| C£® | ĻąĶ¬×“æöĻĀ£¬·“Ó¦2CO+O2ØT2CO2ŹĒŅ»øö·ÅČČ·“Ó¦£¬Ōņ·“Ó¦2CO2ØT2CO+O2ŹĒŅ»øöĪüČČ·“Ó¦ | |
| D£® | ĀČ»ÆĒā·Ö½ā³ÉĒāĘųŗĶĀČĘųŹ±ŠčŅŖĪüŹÕÄÜĮ棬ŹµŃéĀČ»ÆĒāµÄ×ÜÄÜĮæøßÓŚĒāĘųŗĶĀČĘųµÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4 | B£® | CO2 | C£® | H2S | D£® | HCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé ×é | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖł ŠčŹ±¼ä/min | ||
| CO | H2O | H2 | CO2 | |||
| ¢ń | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
| ¢ņ | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
| ¢ó | 900 | a | b | c | d | t |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬1 mol SO3µÄĢå»żŌ¼ĪŖ22.4L | |
| B£® | 1 molÄĘŌ×ÓÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖNA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬17g NH3ŗ¬ĒāŌ×ÓŹżÄæĪŖ3NA | |
| D£® | 1molFeÓė×ćĮæµÄĀČĘų·“Ó¦Ź±£¬×ŖŅʵĵē×ÓŹżŹĒ2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCOOC2H5 | B£® | CH3COOC2H5 | C£® | C6H12O6 | D£® | £ØC6H10O5£©n |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com