
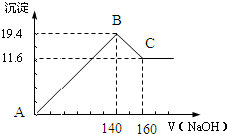
���� ��1����ͼ��֪����A��B��������������ҺΪ140mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ټ��������ƣ����������ܽ⣻
��2���Ӽ�������������Һ�Ϳ�ʼ������������������������ҺΪ140mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ý�������������140mL�����������غ��֪3n[Al��OH��3]+2n[Mg��OH��2]=n��NaOH��=0.14L��5mol/L=0.7mol���Ӽ�������������Һ140mL��160mL�ܽ������������ýη�����ӦAl��OH��3+NaOH=NaAlO2+2H2O������n[Al��OH��3]=��0.16L-0.14L����5mol/L=0.1mol��������ʽ����n[Mg��OH��2]����Ԫ���غ��֪n��Mg��=n[Mg��OH��2]�������Mg��Al�����ʵ���֮�ȣ���������������ҺΪ140mLʱ�����������ʱΪMg��OH��2��Al��OH��3����ҺΪ�Ȼ�����Һ��������Ԫ���غ��ʱ��Һ��n��NaCl��=n��NaOH�����ݴ˼����n��HCl����
��� �⣺��1����ͼ��֪����A��B��������������ҺΪ140mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ټ��������ƣ����������ܽ⣬��BC�η�Ӧ�����ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��2����ͼ��֪���Ӽ�������������Һ�Ϳ�ʼ������������������������ҺΪ140mLʱ�����������ʱΪMg��OH��2��Al��OH��3���ý�������������140mL�����������غ��֪3n[Al��OH��3]+2n[Mg��OH��2]=n��NaOH��=0.14L��5mol/L=0.7mol���Ӽ�������������Һ140mL��160mL�ܽ������������ýη�����ӦAl��OH��3+NaOH=NaAlO2+2H2O������n[Al��OH��3]=��0.16L-0.14L����5mol/L=0.1mol����3��0.1mol+2n[Mg��OH��2]=0.7mol����ã�n[Mg��OH��2]=0.2mol����Ԫ���غ��֪n��Mg��=n[Mg��OH��2]=0.2mol��n��Al��=n[Al��OH��3]=0.1mol��n��Mg����n��Al��=0.2mol��0.1mol=2��1��
���������ʱ����ҺΪ�Ȼ�����Һ��������Ԫ���غ��ʱ��Һ��n��NaCl��=n��NaOH��=0.16L��5mol/L=0.8mol��������Ԫ���غ�n��HCl��=0.8mol������������ʵ���Ũ��Ϊ$\frac{0.8mol}{0.2L}$=4mol/L��
��Mg��Al�����ʵ���֮��Ϊ2��1����������ʵ���Ũ��Ϊ4mol/L��
���� ���⿼��þ�����������ʡ������ļ��㣬��ͼ�������ʽ���飬��Ŀ�Ѷ��еȣ�����ͼ����εķ����ķ�Ӧ�ǽ���ؼ����������غ���㣮


 ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8 | B�� | 6 | C�� | 5 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼���ơ��������ơ��Ȼ��� | B�� | �Ȼ������������ơ�̼���� | ||
| C�� | �������ơ�̼���ơ��Ȼ��� | D�� | ̼���ơ��Ȼ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
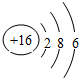
 ijͬѧ���о�ǰ18��Ԫ��ʱ���֣����Խ������ų���ͼ��ʾ�ġ���ţ����״��ͼ��ÿ����•������һ��Ԫ�أ�����O�������Ԫ�أ�����˵���д�����ǣ�������
ijͬѧ���о�ǰ18��Ԫ��ʱ���֣����Խ������ų���ͼ��ʾ�ġ���ţ����״��ͼ��ÿ����•������һ��Ԫ�أ�����O�������Ԫ�أ�����˵���д�����ǣ�������| A�� | ��O��ԽԶ��Ԫ��ԭ�Ӱ뾶Խ�� | |
| B�� | ����������Ԫ�ش���ͬһ�� | |
| C�� | BԪ����ͼ�н�������ǿ��Ԫ�� | |
| D�� | A��B��ɵĻ��������������ӵĸ����ȶ���1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��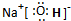 �����ֻ������γɵľ����������Ļ�ѧ�����������Ӽ������ۼ���
�����ֻ������γɵľ����������Ļ�ѧ�����������Ӽ������ۼ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2S2O3��Һ�������Ե�ԭ���ǣ�H2S2O3?H++HS2O3- | |
| B�� | Na2S2O3��Һ�Լ��Ե�ԭ���ǣ�S2O32-+2 H2O?H2S2O3+2OH- | |
| C�� | Na2S2O3��AgBr��Ӧ�����ӷ���ʽ�ǣ�2S2O32-+AgBr?Ag��S2O3��23-+Br- | |
| D�� | ��Ӱ���������Խ�ǿ����Һ�н��е�ԭ���ǣ�S2O32-+2H+=S��+SO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��С��Ӧ��Ũ�ȣ��ɼ�С��Ӧ������еĻ���Ӱٷ�����ʹ��Ч��ײ������С | |
| B�� | �����¶���ʹ��ѧ��Ӧ����������Ҫԭ���������˷�Ӧ������л���ӵİٷ��� | |
| C�� | ������μӵĻ�ѧ��Ӧ��������ѹǿ������С��Ӧ�������ݻ����������ӻ���ӵİٷ������Ӷ�ʹ��Ӧ�������� | |
| D�� | ������Ӱ�췴Ӧ��ܵ�������λ����ڻ���Ӱٷ������Ӷ�����Ӧ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com