


科目:高中化学 来源:北京市海淀区2012届高三5月查漏补缺化学试题 题型:022
下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物.
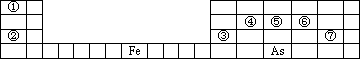
Ⅰ.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去).
(1)若E为氧化物,则A的化学式为________,A与水反应的化学方程式________,该反应中氧化剂和还原剂的物质的量之比为________.
①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为________,用电子式表示C的形成过程:________.
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为________.
(2)若E为单质气体,D为白色沉淀,A的化学式可能是________,B含有的化学键类型为________,C与X反应的离子方程式为________.
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该可逆反应的化学方程式为________.t℃时,在密闭恒容的某容器中投入等物质的量的D和水蒸气,一段时间后达平衡,该温度下反应的平衡常数K=1,D的转化率为________.
Ⅱ.元素周期表是人们研究物质性质的重要工具
(1)列举一条能够说明⑤的非金属性强于④的事实:________,
从原子结构的角度解释⑤的非金属性强于④的原因:________.
(2)As在元素周期表中的位置:________.
(3)As的原子结构示意图为________,其氢化物的化学式为________.
(4)Y由②⑥⑦三种元素组成,它的水溶液是生活中常见的消毒剂.As可与Y的水溶液反应,生成H3AsO4,当消耗1 mol氧化剂时,电子转移了2 mol,该反应的化学方程式为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
A.标准状况下,
B.1 mol铁丝在1 mol Cl2中充分燃烧时转移的电子数为3NA
C.向某密闭容器中通入2 mol SO2和1 mol O2,在高温和催化条件下充分反应后容器内分子总数为2NA
D.等体积等物质的量浓度的K2CO3溶液与K2SO4溶液中离子总数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
某容器中含有22.4 L O2,下列叙述一定正确的是
A. 气体质量为32g B. 约含有6.02×1023个O2分子
C. 气体的物质的量为1mol D. 红热的铁丝可在其中剧烈燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com