
| A.铁 | B.铜 | C.钠 | D.铅 |
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源:不详 题型:填空题
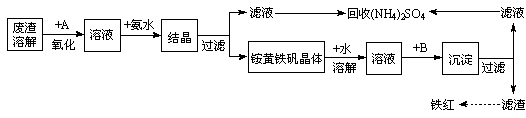
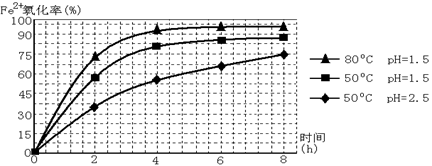
| A.空气 | B.Cl2 | C.MnO2 | D.H2O2, |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
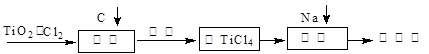
| 物质 | TiCl4 | FeCl3 | SiCl4 | AlCl3 |
| 沸点/℃ | 136 | 310 | 56.5 | 180 |
 TiCl4(g)+2CO (g) 。试计算其反应的△H= kJ?mol-1;反应的平衡常数表达式K= ,在下图中作出TiCl4达到平衡后百分含量随温度的变化趋势图。
TiCl4(g)+2CO (g) 。试计算其反应的△H= kJ?mol-1;反应的平衡常数表达式K= ,在下图中作出TiCl4达到平衡后百分含量随温度的变化趋势图。
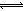 TiCl4(l)+O2(g)△H=+151kJ?mol-1。该反应在高温条件下但难以发生,但加入碳后反应能顺利进行,试解析上述原因
TiCl4(l)+O2(g)△H=+151kJ?mol-1。该反应在高温条件下但难以发生,但加入碳后反应能顺利进行,试解析上述原因 查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
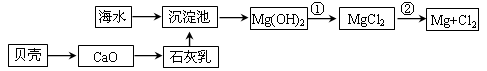
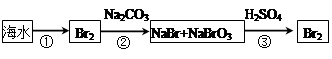

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等 |
| B.将卤水中Mg2+转化为氢氧化镁沉淀通常是向卤水加入氢氧化钠溶液 |
| C.直接加热MgCl2·6H2O可得到较纯净的无水MgCl2 |
| D.在高温下用铝还原MgCl2可制取金属镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(1)(3)(4)(5) | B.(2)(3)(5)(6) | C.(3)(4)(5)(6) | D.(1)(2)(3)(4) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
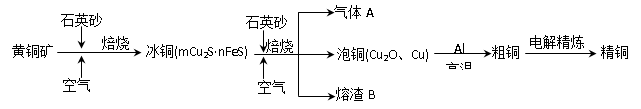
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.减少一次性用品的使用 |
| B.利用太阳能蒸馏海水进行海水的淡化 |
| C.避开公共交通的拥挤,倡导自驾出行 |
| D.海水和淡水交汇处安装半透膜,利用水中电解质浓度的差异进行发电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com