
 H++B(OH)4-���÷�Ӧ�еļ��� ����H3BO3��H2O����
H++B(OH)4-���÷�Ӧ�еļ��� ����H3BO3��H2O���� �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������������Ա�̼�������� NaHS��Һ�У� c��Na+����c��HS������c��H+����c��OH���� |
| B�����������ʵ���Ũ����ͬ��NH4Cl��NH3��H2O�����ҺpH��7������pH=7��NH4Cl��NH3��H2O�����Һ�У�c��NH4+����c��NH3��H2O�� |
| C��Na2HPO4��Һ�У�c��H+�� + c��H2PO4-�� + 2c��H3PO4�� ="=" c��PO43-�� + c��OH-�� |
| D��5mL0��1mol/LAgNO3��Һ��1mL 0��1mol/LAlCl3��Һ��Ϻ����Һ�У� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��һԪǿ�� | B����Ԫǿ�� | C���κ�ǿ�� | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��HCO3��+ H2O  H3O+ + CO32�� H3O+ + CO32�� |
B��NH3 + H2O  NH4�� + OH�� NH4�� + OH�� |
C��CO32��+2H2O  H2CO3 + 2OH�� H2CO3 + 2OH�� |
D��Al3+ +3H2O  Al(OH)3+3H+ Al(OH)3+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ˮ���Ȼ�淋Ļ��Һ����pH=7ʱ��c��Clһ��>C��NH4+�� |
| B��pH=2��һԪ���pH=12��NaOH��Һ��������,���Һ��C��H+��һ�� ����C��OH-�� |
| C��0.1mol��L��Na2S��Һ�У�C��OH����=c��H+��+C��HS����+2C��H2S�� |
| D��0.1mol��LNaCl��Һ��0.1mol/LNaF��Һ����������Ũ��һ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1 mol/L NH4Cl��Һ�м���NH 3��H2O ��������ʱ��c(NH4�� )��c(Cl��) |
| B��0.1 mol/L Na2CO3��Һ�У�c(OH��)��c(H��)��c(HCO3��)��2c(H2CO3) |
| C������������Һ�еμ�ϡ����õ���pH��3�Ļ����Һ�У�c(Na��)��c(NO3)�� |
| D��CH3COONa��Һ�м�������CH3COOH���������Ի����Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��C(Na+)>C(CO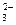 )>C(HCO )>C(HCO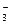 )>C(OH-)>C(H+) )>C(OH-)>C(H+) |
B��2C(Na+)=3[C(CO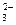 )+C(HCO )+C(HCO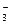 )+C(H2CO3)] )+C(H2CO3)] |
C��2C(OH-)+C(CO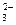 )=C(HCO )=C(HCO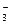 )+3C(H2CO3)+2C(H+) )+3C(H2CO3)+2C(H+) |
D��C(Na+)+C(H+)=C(OH-)+C(HCO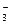 )+2C(CO )+2C(CO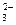 ) ) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com