
| A、1.8mol | B、2mol | C、2.2 mol | D、2.4mol |
| 5 |
| 3 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.![]() mol B.
mol B.![]() mol C.
mol C.![]() mol D.
mol D.![]() mol
mol
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 2.3硫酸工业练习卷(解析版) 题型:选择题
在一定条件下,某密闭容器发生如下反应:2SO2(g)+O2(g) 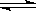 2SO3(g) , △H=
-98.3kJ/mol,反应达到平衡后SO2、O2、SO3的物质的量之比为3:2:5,保持其它条件不变,升温后重新达到平衡,SO3、O2的物质的量分别为2α mol和α mol,则此时容器内SO2的物质的量应为( )。
2SO3(g) , △H=
-98.3kJ/mol,反应达到平衡后SO2、O2、SO3的物质的量之比为3:2:5,保持其它条件不变,升温后重新达到平衡,SO3、O2的物质的量分别为2α mol和α mol,则此时容器内SO2的物质的量应为( )。
A.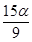 mol B.
mol B. mol C.
mol C.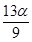 mol D.
mol D.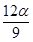 mol
mol
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
在一定条件下,某密闭容器内,SO2氧化成SO3的热化学方程式为:2SO2(g)+O2(g) 2SO3(g) △H =-a kJ·mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是( )
2SO3(g) △H =-a kJ·mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是( )
A.4mol SO2和2mol O2 B.5mol SO2和3mol O2
C.4mol SO2和4mol O2 D.4mol SO2、2mol O2和2mol SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com