
【题目】某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L.
阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
阴离子 | Cl﹣ CO32﹣ NO3﹣ SO42﹣ SiO32﹣ |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是 .
(3)将Ⅲ中红棕色气体(标况下)收集一满试管然后倒扣入水中(假设溶质不扩散),所得溶液的物质的量浓度为mol/L(精确到千分位)
(4)甲同学最终确定原溶液中所含阳离子是 , 阴离子是 . (写离子符号)(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为g.
【答案】
(1)K+、Fe3+
(2)3Fe2++NO3﹣+4H+=3Fe3++NO↑+2H2O
(3)0.045
(4)Fe2+、Cu2+;Cl﹣、NO3﹣、SO42﹣;1.6
【解析】解:Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察),说明没有K+ . Ⅱ.取少量溶液,加入KSCN溶液无明显变化,说明没有Fe3+ .
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变,说明 Fe2+与NO3﹣和H+反应生成NO,即溶液中有Fe2+、NO3﹣ , 加盐酸溶液中阴离子种类不变,说明原溶液中有Cl﹣ , 加盐酸溶液依然澄清加盐酸说明没有SiO32﹣;
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成,说明有SO42﹣;(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+ ,
所以答案是:K+、Fe3+;(2)Ⅲ中加入少量盐酸生成无色气体,是Fe2+与NO3﹣和H+反应生成NO,其离子方程式:3Fe2++NO3﹣+4H+═3Fe3++NO+2H2O;
所以答案是:3Fe2++NO3﹣+4H+═3Fe3++NO+2H2O;(3)标准状况下,将一充满NO2气体的试管,倒扣于水中,至液面不再升高时,再充入氧气可以使液面继续上升至充满试管,最后得到的硝酸,设试管体积为VL,最终试管中所得溶液的浓度为 ![]() =0.045mol/L,
=0.045mol/L,
所以答案是:0.045;(4)由以上推断可知溶液中阴离子为 Cl﹣、NO3﹣、SO42﹣ , 且各为0.1mol/L;已经推断出的阳离子是Fe2+ , 其浓度为0.1mol/L,由电荷守恒可知溶液中还有一种+2价阳离子,所以还有Cu2+ , 所以甲同学最终确定原溶液中所含阳离子是:Fe2+、Cu2+;阴离子是:Cl﹣、NO3﹣、SO42﹣;
所以答案是:Fe2+、Cu2+;Cl﹣、NO3﹣、SO42﹣;(5)另取100mL原溶液,加入足量的NaOH溶液,Fe2+生成Fe(OH)2 , 又被氧气氧化为Fe(OH)3 , Cu2+生成Cu(OH)2 , 充分反应后过滤,洗涤,灼烧至恒重,得到的固体为Fe2O3和CuO,
根据元素守恒:n(CuO)=n(Cu2+)=cV=0.1mol/L×0.1L=0.01mol;n(Fe2O3)= ![]() n(Fe2+)=0.005mol,
n(Fe2+)=0.005mol,
所以固体质量为:m(CuO)+m(Fe2O3)=0.01mol×80g/mol+0.005mol×160g/mol=1.6g,
所以答案是:1.6g.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】控制变量是科学研究的重要方法。相同质量的铁与足量稀硫酸分别在下列条件下发生反应,其中化学反应速率最大的是
选项 | 硫酸浓度 | 反应温度 | 铁的状态 |
A | 2.0 mol/L | 20℃ | 块状 |
B. | 0.5 mol/L | 20℃ | 粉末状 |
C. | 1.0 mol/L | 40℃ | 块状 |
D. | 2.0 mol/L | 40℃ | 粉末状 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选取萃取剂将溴水中的溴萃取出来,这种萃取剂必须具备的性质是( )
A. 不溶于水,但必须与溴发生反应 B. 不溶于水,但比水更容易溶解溴
C. 不溶于水,且密度必须比水大 D. 不溶于水,且密度必须比水小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物异搏定路线中某一步骤如图,下列说法正确的是( ) 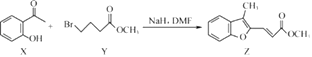
A.物质 X在空气中不易被氧化
B.物质 Y中只含一个手性碳原子
C.物质 Z中所有碳原子不可能在同一平面内
D.等物质的量的 X,Y分别与 NaOH反应,最多消耗 NaOH的物质的量之比为 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物分子式为C4H8 , 据此推测其结构和性质不可能的是( )
A.它与乙烯可能是同系物
B.一氯代物只有一种
C.分子结构中甲基的数目可能是0、1、2
D.等质量的CH4和C4H8 , 分别在氧气中完全燃烧,CH4的耗氧量小于C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】赤铜矿的成份是Cu2O,辉铜矿的成份是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu2O+Cu2S ![]() 6Cu+SO2↑,对于该反应,下列说法正确的是.
6Cu+SO2↑,对于该反应,下列说法正确的是.
A.该反应的氧化剂只有Cu2O
B.Cu既是氧化产物又是还原产物
C.每生成1 mol Cu,还原剂转移给氧化剂的电子为2mol
D.该反应中氧化产物与还原产物的质量比为1:6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是.
A.![]() 的一溴代物和
的一溴代物和 ![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
B.CH3CH=CHCH3分子中的四个碳原子在同一直线上
C.按系统命名法,化合物 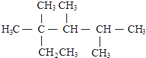 的名称是2,3,4﹣三甲基﹣2﹣乙基戊烷
的名称是2,3,4﹣三甲基﹣2﹣乙基戊烷
D.![]() 与
与 ![]() 都是α﹣氨基酸且互为同系物
都是α﹣氨基酸且互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若实验遇到下列情况.对所配氢氧化钠溶液的物质的量浓度有何影响(填偏高、偏低、无影响).
(1)将氢氧化钠固体放在滤纸上进行称量;
(2)未将洗涤液加入容量瓶;
(3)定容时仰视刻度线;
(4)摇匀后发现凹液面下降,又加蒸馏水至刻度线;
(5)配制前容量瓶用水洗涤后未进行干燥处理;
(6)氢氧化钠溶液未冷却至室温就转移到容最瓶 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com