

分析 B为黑色固体、有磁性,应为Fe3O4,A为无色有毒气体,结合转化关系,可推知A具有还原性,故A为CO,则D为CO2,E为Fe;顺推可知G为NaHCO3,J为Na2CO3,H是FeCl2,K为FeCl3,金属C与Fe3O4反应生成Fe与F,F为金属氧化物,既与盐酸反应又能与氢氧化钠反应,F应为Al2O3,则C是Al,I为AlCl3,L为NaAlO2,结合物质的性质解答该题.
解答 解:B为黑色固体、有磁性,应为Fe3O4,A为无色有毒气体,结合转化关系,可推知A具有还原性,故A为CO,则D为CO2,E为Fe;顺推可知G为NaHCO3,J为Na2CO3,H是FeCl2,K为FeCl3,金属C与Fe3O4反应生成Fe与F,F为金属氧化物,既与盐酸反应又能与氢氧化钠反应,F应为Al2O3,则C是Al,I为AlCl3,L为NaAlO2.
(1)C与氢氧化钠溶液反应的化学方程式:2Al+2 NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2 NaOH+2H2O=2NaAlO2+3H2↑;
(2)B与C高温反应生成E和F的化学方程式为:8Al+3Fe3O4 $\frac{\underline{\;高温\;}}{\;}$ 9Fe+4Al2O3,
故答案为:8Al+3Fe3O4 $\frac{\underline{\;高温\;}}{\;}$ 9Fe+4Al2O3;
(3)过量的D通入到L溶液中的离子方程式为:CO2+AlO2-+2H2O=Al (OH)3↓+HCO3-,
故答案为:CO2+AlO2-+2H2O=Al (OH)3↓+HCO3-.
点评 本题考查无机物的推断,题目难度中等,以A、B为突破口进行推断,侧重考查元素化合物性质,学习中注意把握.


科目:高中化学 来源: 题型:填空题

 .
.
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
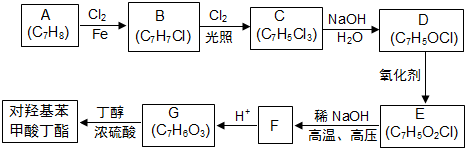
 ; F的分子式为C7H4O3Na2;
; F的分子式为C7H4O3Na2; ,该反应类型为取代反应;
,该反应类型为取代反应;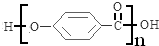 .
.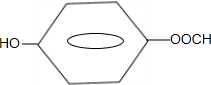 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2gO3和2 gO2 | B. | 9克H2O和0.5NA个CO2 | ||
| C. | 标准状况下1molO2和22.4LH2O | D. | 0.2molH2和4.48LHCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③⑤⑥ | C. | ①③④⑤⑥ | D. | .全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 “低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视.
“低碳循环”、如何降低大气中CO2的含量、有效地开发利用CO2,引起了全世界的普遍重视.| 实验组 | 温度/℃ | 起始量(mol) | 平衡量(mol) | 达到平衡所需要时间/min | ||
| CO(g) | H2O(g) | CO2(g) | H2(g) | |||
| I | 800 | 2 | 2 | x | 1 | 5 |
| II | 900 | 1 | 2 | 0.5 | 0.5 | tm |
| III | 900 | 2 | 4 | y | y | tn |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实 验 用 品 | 溶 液 温 度 | 中和热 △H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HCO3-+H2O?H3O++CO32- | B. | NH4++H2O?NH3•H2O+H+ | ||
| C. | PO43-+H2O═HPO42-+OH- | D. | NH3+H2O?NH4++OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com