
【题目】瓦斯中甲烷与氧气的质量比为1︰4时极易发生爆炸,则此时甲烷与氧气的体积比是( )
A. 1︰4 B. 1︰8 C. 1︰1 D. 1︰2
科目:高中化学 来源: 题型:
【题目】李克强总理在《2018年国务院政府工作报告》中强调“今年二氧化硫、氮氧化物排放量要下降3%。”因此,研究烟气的脱硝(除NOx)、脱硫(除SO2)技术有着积极的环保意义。
(1)汽车的排气管上安装“催化转化器”,其反应的热化学方程式为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min) NO的物质的量随时间变化如图。
2CO2(g)+N2(g) ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min) NO的物质的量随时间变化如图。

①图中a、b分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n (NO)的变化曲线,其中表示催化剂表面积较大的曲线是___________。(填“a”或“b”)
②T℃时,该反应的化学平衡常数K=_______________;平衡时若保持温度不变,再向容器中充入CO、CO2各0.2 mol,则平衡将_________移动。(填“向左”、“向右”或“不”)
③15min时,若改变外界反应条件,导致n (NO)发生图中所示变化,则改变的条件可能是_______________________________________________ (任答一条即可)。
(2)在催化剂作用下,用还原剂[如肼(N2H4)]选择性地与NOx反应生成N2和H2O。
已知200℃时:Ⅰ.3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1;
II. N2H4(g)+H2(g) =2NH3(g) ΔH2=-41.8 kJ·mol-1。
①写出肼的电子式:____________________。
②200℃时,肼分解成氮气和氢气的热化学方程式为:_____________________________。
③目前,科学家正在研究一种以乙烯作为还原剂的脱硝原理,其脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如下图所示。

为达到最佳脱硝效果,应采取的条件是_________________________________________。
(3)利用电解装置也可进行烟气处理,如图可将雾霾中的NO、SO2分别转化为NH4+和SO42-,阳极的电极反应式为____________________________;物质A是______________ (填化学式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的电离方程式正确的是 ( )
A. NaOH=Na+ + O2— + H+ B. H2SO4=H2+ + SO42—
C. MgCl2 = Mg2++2Cl— D. Al2(SO4)3=2Al3+ + 3(SO42—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是我国规定的食盐补碘剂,利用“KClO3氧化法”可制备KIO3,流程如下:
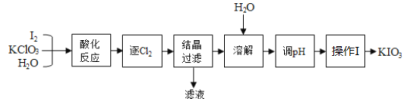
已知:“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。
(1)KIO3所含的化学键有______________________。
(2)逐出的Cl2可用_________________检验;“滤液”中的溶质主要是____________;“调pH”中所用的试剂是_________________。
(3)已知KIO3在水中的溶解度随温度升高而增大,则操作I包含的操作应该是_______、_______、过滤。
(4)为测定“加碘食盐”中碘元素含量:①称取50.000g食盐,配成250mL溶液;②量取25.00mL溶液于锥形瓶中,加入足量KI,并用少量稀硫酸酸化,使KIO3与KI反应完全;③以淀粉为指示剂,用2.0×10-4mol/L的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液体积为30.00mL。已知:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),2Na2S2O3+I2→Na2S4O6+2NaI。测定过程中,所需仪器在使用前必须检查是否漏液的有________________。
(5)判断滴定终点的依据是________________________________。
(6)配平:KIO3+KI+H2SO4→K2SO4+I2+H2O ____________
(7)该食盐中碘元素的含量是_________mg/kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭烧瓶中,25 ℃时存在着平衡:2NO2(g)![]() N2O4(g)(正反应放热)。把烧瓶置于100 ℃的水中,则下列几项性质中不会改变的是
N2O4(g)(正反应放热)。把烧瓶置于100 ℃的水中,则下列几项性质中不会改变的是
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
A. ①和③ B. ②和④ C. ④和⑤ D. ③和⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请应用化学反应原理的相关知识解决下列问题
(1)已知NaCl的溶解热为3.8kJ·mol-1(吸热)
Na(s)-e-====Na+(aq) △H=-240 kJ/mol
![]() Cl2(g)+e-====Cl-(aq) △H=-167 kJ/mol
Cl2(g)+e-====Cl-(aq) △H=-167 kJ/mol
写出钠在氯气中燃烧的热化学方程式_______________________。
(2)一定条件下,在2L恒容密闭容器中充入1.5 mol CO2和3molH2发生反应:CO2(g)+3H2(g) ![]() CH3OH(g) +H3O(g)
CH3OH(g) +H3O(g)
下图是反应体系中CO2的平衡转化率与温度的关系曲线。已知在温度为500K的条件下,该反应l0min达到平衡;
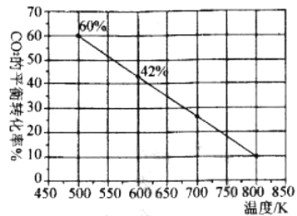
①该反应是__________ (填“吸热”或“放热”)反应。
②在0~10min时段反应速率v(H2)为__________。
③若改充入2 mol CO2和3molH2,图中的曲线会__________(填“上移”或“下移”)。
(3)根据下表数据回答问题:
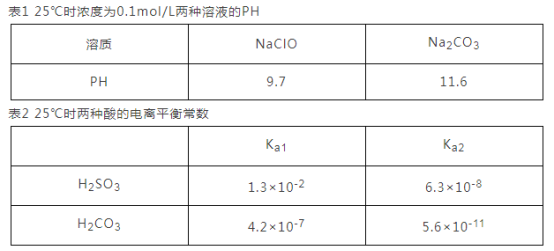
①根据表1能不能判断出H2CO3与HClO酸性强弱? _________(填“能”或“不能”)。
②0.10mol·L-lNa2SO3溶液中离子浓度由大到小的顺序为___________________________。
③H2SO3溶液和 NaHCO3溶液反应的离子方程式为________________________________。
(4)已知:t℃时,Ksp(AgCl)=1.5×10-10、Ksp (Ag2CrO4)=2.0×10-12;AgCl为白色沉淀,Ag2CrO4为砖红色沉淀,t℃时,向Cl-和CrO42-浓度均为0.1mol/L的混合溶液中逐滴加入AgNO3溶液至过量且不断搅拌,实验现象为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同的A、B密闭容器中分别充入2 mol SO2和1 mol O2,使它们在一定温度下反应,并达新平衡:2SO2+O2![]() 2SO3(g)。若A容器保持体积不变,B容器保持压强不变。当A中SO2的转化率为25%时,B中SO2的转化率为
2SO3(g)。若A容器保持体积不变,B容器保持压强不变。当A中SO2的转化率为25%时,B中SO2的转化率为
A. 25%B. 大于25%
C. 小于25%D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g) ![]() CH4(g)+2O2(g) ΔH=+802KJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线。下列说法正确的是
CH4(g)+2O2(g) ΔH=+802KJ/mol,下图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线。下列说法正确的是
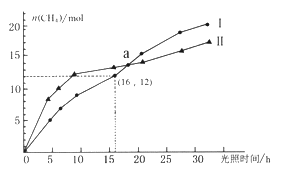
A. 0-15h内,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好
B. 反应开始后的30h内,第Ⅰ种催化剂的作用下,反应吸收的热量多
C. a点时,CO2的转化率相等
D. 0-16h内,v(O2)=1.5mol/(L·h)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二氯化二硫(S2C12)是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为l93K,沸点为41lK,遇水反应产生的气体能使品红褪色。下列有关说法正确的是
A. S2C12晶体中存在离子键B. S2C12在熔融状态下能导电
C. S2C12分子中各原子均达到8电子稳定结构D. S2C12与水反应不属于氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com