
 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.分析 根据反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”分析,在反应中,Cu被氧化,失电子,应为原电池的负极,电极反应为Cu-2e-=Cu2+,则正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,电解质溶液为AgNO3 ,原电池中,电子从负极经外电路流向正极.
解答 解:(1)由反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,Ag+在正极上得电子被还原,电解质溶液为AgNO3 ,
故答案为:Cu;AgNO3;
(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,
故答案为:正; Ag++e-=Ag; Cu-2e-=Cu2+;
(3)原电池中,电子从负极经外电路流向正极,本题中由Cu极经外电路流向Ag极,故答案为:铜;银;
(4)X电极上发生的反应为Cu-2e-=Cu2+,当外电路中通过0.2mol电子时,反应的Cu的质量为6.4g,故答案为:6.4.
点评 本题考查原电池的设计及工作原理,注意电极反应式的书写方法,牢固掌握原电池中电极的判断,电极反应式的书写的方法性问题.


科目:高中化学 来源: 题型:选择题
| A. | 2:3:2 | B. | 2:3:3 | C. | 1:3:2 | D. | 3:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
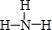 .
. ;一种由B、C组成的化合物与AC2电子总数相等,其化学式为N2O.
;一种由B、C组成的化合物与AC2电子总数相等,其化学式为N2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去暖水瓶中的水垢 | |
| B. | 用热的纯碱溶液洗涤餐具上的油 | |
| C. | 用米汤检验食盐中是否含碘酸钾 | |
| D. | 用灼烧并闻气味的方法区别纯棉和纯羊毛织物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸 | B. | 氢氧化钠溶液 | C. | FeCl3溶液 | D. | 高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | W | X | Y | Z |
| 性质或结构信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远. | 工业上通过分离液态空气获得其单质.原子的最外层未达到稳定结构. | 单质常温常压下是气体,原子的M层差一个电子达稳定结构. | +2价阳离子的核外电子排布与氖原子相同. |
| A. | 上表中与W属于同一周期的元素是Z和Y | |
| B. | Z和Y形成的化合物属于离子化合物 | |
| C. | X的氢化物常温、常压下一定为液体 | |
| D. | Y单质为有色气体,具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18O、19O、24Mg | B. | 12C、31P、27Al | C. | 第ⅤA族原子 | D. | 第三周期原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
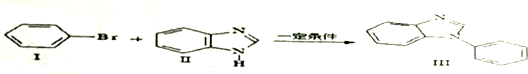
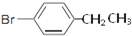 、
、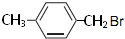 .
.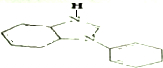 .
.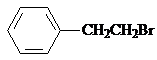 ,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为:
,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为: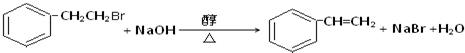 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素名称 | 氟 | 氧 | 溴 | 碘 |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
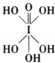 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4.(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4.(填“>”、“<”或“=”)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com