
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
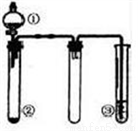
选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D
科目:高中化学 来源:2016-2017学年宁夏银川市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A. 乙烯中C=C键的键能是乙烷中C—C键键能的2倍
B. 氮气分子中含有1个σ键和2个π键
C. N—O键的极性比C—O键的极性大
D. NH4+中4个N—H键的键能不相同
查看答案和解析>>
科目:高中化学 来源:2017届上海市普陀区高三第二学期质量调研(二模)化学试卷(解析版) 题型:实验题
实验室中模拟纯碱工业制法,进行了如下三步实验:①将CO2、NH3通入H2O中制得NH4HCO3,②NH4HCO3和饱和食盐水反应生成小苏打,③将小苏打制成纯碱。
(1)步骤①先通入水中的气体是______。析出NH4HCO3的反应有两步,第二步反应的离子方程式为____________________。
(2)步骤②生成了含少量NaCl的小苏打,现用滴定法测定其中NaHCO3的含量。过程为:称取一定质量样品,配成250mL溶液,取出25.00mL用0.1000mol/L的盐酸滴定。实验中所写的定量仪器除滴定管外,还有_______、_______。所用的指示剂是______________。
(3)步骤②生成了含少量NaHCO3的纯碱。若用重量法(限用试剂:稀盐酸)测定其中Na2CO3含量,请设计实验方案:_______________________。若该样肠中NaHCO3含量的准确值为99.5%,而上述实验结果为97.6%,则测定的相等误差为___________,可能造成该实验误差的原因是________________。
查看答案和解析>>
科目:高中化学 来源:2017届上海市普陀区高三第二学期质量调研(二模)化学试卷(解析版) 题型:选择题
为了检验某固体物质中是否含有NH4+,一定用不到的试剂或试纸是
A. NaOH溶液 B. 浓盐酸 C. 稀硫酸 D. 红色石蕊试纸
查看答案和解析>>
科目:高中化学 来源:2017届山西省太原市高三模拟考试(一)理综化学试卷(解析版) 题型:填空题
CuSO4和Cu(NO3)2是自然界中重要的铜盐。回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子基态核外电子排布式为_________,S、O、N三种元素的第一电离能由大到小的顺序为_________。
(2)往Cu(NO3)2溶液中通入足量NH3能生成配合物[Cu(NH3)4] (NO3)2。其中NO3-中心原子的杂化轨道类型为_________,[Cu(NH3)4]NO3)2中存在的化学键类型除了极性共价键外,还有_________。
(3)在硫酸铜溶液中加入过量KCN能生成配离子[Cu(CN)4]2-,CN-中提供孤电子对的原子是_________, lmol CN-中含有的π键的数目为_________。与CN-互为等电子体的离子有_________ (写出一种即可)
(4)CuSO4的熔点为560°C,,Cu(NO3)2的溶点为115°C,CuSO4溶点更高的原因是_________。
(5)利用CuSO4和NaOH制备的Cu(OH)2检验醛基时,生成红色的Cu2O ,其晶胞结构如图所示。
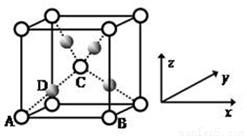
该晶胞原子坐标参数A为(0,0,0);B为(1,0,0) ;C为( ,
, ,
, )。则D原子的坐标参数为_________,它代表_________原子(填元素符号)。
)。则D原子的坐标参数为_________,它代表_________原子(填元素符号)。
②已知金属铜的堆积方式是面心立方最密堆积,则晶体中铜原子的配位数是_________,该晶胞中Cu原子的空间利用率是_________。
查看答案和解析>>
科目:高中化学 来源:2017届山西省太原市高三模拟考试(一)理综化学试卷(解析版) 题型:选择题
化学与材料、生活和环境密切相关,下列说法正确的是( )
A. 糖类、油脂、蛋白质都可发生水解
B. 天然纤维、聚酯纤维、光导纤维都属于有机高分子材料
C. 大力实施矿物燃料脱硫、脱硝技术以减少硫、氮氧化物排放
D. 镀锌铁或镀锡铁镀层破损后仍将通过牺牲阳极的阴极保护法防止腐蚀
查看答案和解析>>
科目:高中化学 来源:2017届山东省济南市高三第一次模拟考试理科综合化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 常温下用二氧化锰和浓盐酸反应制取Cl2
B. 用饱和氯化钠溶液可以洗涤除去氯化钠固体表面少量氯化钾杂质
C. 向某溶液中加入盐酸酸化的BaCl2溶液,产生白色沉淀,可知该溶液中一定含有SO42-
D. 向浓度均为0.01mol/L的K2SO4和KI混合溶液中滴加Pb(NO3)2溶液,先生成PbI2黄色沉淀[已知:Ksp (PbSO4)=1.8×10-8,Ksp ( PbI2)=7.l×10-9]
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高一下学期第一次月考化学试卷(解析版) 题型:选择题
a、b、c表示相应仪器中加入的试剂,可用如图装置制取、净化、收集的气体是
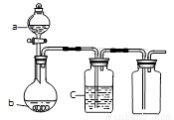
编号 | 气体 | a | b | c |
A | SO2 | 浓H2SO4 | 铜屑 | 饱和Na2SO3溶液 |
B | CO2 | 稀HNO3 | 碳酸钙 | 饱和NaHCO3 |
C | NO | 稀HNO3 | 铜屑 | H2O |
D | NO2 | 浓HNO3 | 铜屑 | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二3月月考化学试卷(解析版) 题型:选择题
0.01mol氯化铬(CrCl3·6H2O)在水溶液中用过量的AgNO3处理,产生0.02mol AgCl沉淀,此氯化铬最可能是( )
A.[Cr(H2O)6]Cl3 B.[Cr(H2O)5Cl]Cl2·H2O
C.[Cr(H2O)4Cl2]Cl·2H2O D.[Cr(H2O)3Cl3]·3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com