
在标准状况下①6.72LCH4 ②3.01×1023个HCl分子 ③13.6gH2S ④0.2molNH3,下列对这四种气体的关系从大到小表达正确的是
a.体积②>③>①>④ b.密度②>④>③>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abc B.bcd C.abcd D.acd
 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学b卷(解析版) 题型:选择题
甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙→沉淀;甲+丙→沉淀;乙+丙→沉淀;丙十丁→沉淀;乙+丁→无色无味气体。则甲、乙、丙、丁四种溶液依次是
A.BaCl2 、Na2CO3、盐酸 、AgNO3 B.BaCl2 、Na2CO3、、AgNO3 、盐酸
C.Na2CO3、 盐酸 、AgNO3、 BaCl2 D.AgNO3、盐酸、 BaCl2、Na2CO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
关于容量瓶的四种叙述:①是配制一定质量分数溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是
A. ①②③④ B. ②③ C. ①②④ D. ②③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
下列实验操作正确的是
A. 当某实验没有准确的药品用量说明时,为看到明显现象,取用药品越多越好
B. 取用细口瓶里的试液时,先拿下瓶塞,倒放在桌上,然后标签朝外拿起瓶子,瓶口要紧挨着试管口,将液体缓缓地倒入试管
C. 胶头滴管取完一种试液后,可直接取另一种不与其反应的试液
D. 取用粉末状固体或固体小颗粒时,应用钥匙或纸槽,取用块状固体时,应用镊子夹取
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴危险警告标签。下面所列物质中,贴错了标签的是
| A | B | C | D |
物质的化学式 | H2SO4(浓) | C2H5OH(酒精) | Hg(汞) | NaCl |
危险警告标志 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
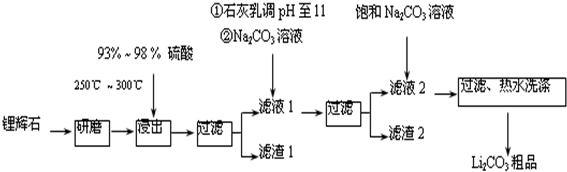
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
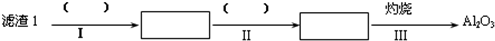
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
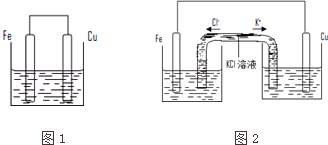
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含NA个H的H2的物质的量为1 mol | |
| B. | NA个CO和1 mol N2所含分子数相等 | |
| C. | NA个H2SO4与1 mol H3PO4所含氢原子的个数比为1:1 | |
| D. | 0.1 mol C含1.2NA个质子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com