
| A、焰色反应 |
| B、节日里燃放的焰火 |
| C、金属导线可以导电 |
| D、夜空中的激光 |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| A、取代→加成→氧化→消去 |
| B、取代→水解→消去→氧化 |
| C、加成→水解→氧化→氧化 |
| D、加成→取代→消去→还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
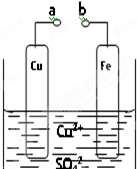 某学习小组为研究原电池原理,设计如图装置.叙述错误的是( )
某学习小组为研究原电池原理,设计如图装置.叙述错误的是( )| A、a和b不连接时,铁片上会有金属铜析出,质量增重 |
| B、a和b用导线连接时,铜片上发生的反应为:Cu2++2e-═Cu |
| C、a和b用导线连接时,Cu2+移向Fe,电子在溶液中从负极移向正极 |
| D、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该一元酸溶液的pH=1 | ||
| B、该溶液中水的离子积常数为1×10-22 | ||
| C、该溶液中HA的电离度为 0.1% | ||
D、若加水稀释,则
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将40gNaOH溶解在1L水中 |
| B、将1L10mol/L的浓盐酸加入9L水中 |
| C、将常温常压下22.4L HCl气体溶于水配成1L溶液 |
| D、将40g NaOH溶解在少量水中,再加蒸馏水定容到溶液体积为1L |
查看答案和解析>>
科目:高中化学 来源: 题型:
48 22 |
| A、大于 | B、小于 |
| C、等于 | D、不能肯定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氢的质量是1g |
| B、1molCO的质量为28g?mol-1 |
| C、阿伏加德罗常数等于6.02×1023 |
| D、3.01×1023个SO2分子约是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
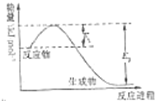 氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题:| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com