
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
分析 根据阿伏加德罗定律,同温同压下,相同体积的任何气体都含有相同的分子数,结合n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$解答.
解答 解:同温、同压下,气体的Vm相等,则体积相同时,n=$\frac{V}{Vm}$可知,两种气体的物质的量相同,设物质的量都为n,则:
①m(N2O)=nM=44n,m(CO2)=nM=44n,故①正确;
②N(C)=nNA,N(N)=2n(N2O)×NA=2NA,所含碳原子数与氮原子数不相等,故②错误;
③N(N2O)=nNA,N(CO2)=nNA,所含分子数相等,故③正确;
④1个N2O含有22个质子,1个CO2含有22个质子,所以二者物质的量相等时,其质子数相等,故④正确;
故选:D.
点评 本题考查阿伏加德罗定律,题目难度不大,注意同温同压下,相同体积的任何气体都含有相同的分子数,把握有关物质的量与体积、质量、分子数目的相关计算公式的运用.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
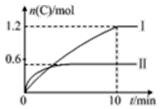 在2L的恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1,实验内容和结果分别如表和图所示,下列说法正确的是( )
在2L的恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1,实验内容和结果分别如表和图所示,下列说法正确的是( )| 实验 序号 | 温度 | 起始物质的量 | 热量 变化 | |
| A | B | |||
| Ⅰ | 600℃ | 1 mol | 3 mol | 96 kJ |
| Ⅱ | 800℃ | 1.5 mol | 0.5 mol | -- |
| A. | 上述方程式中a=-160 | |
| B. | 实验Ⅰ中,10 min内平均速率v(B)=0.06 mol•L-1•min-1 | |
| C. | 600℃时,该反应的平衡常数是0.45 | |
| D. | 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol羟基与1mol氢氧根离子所含有的电子数目均为9NA | |
| B. | 电解饱和食盐水,当阴极产生2.24L气体时,转移的电子数为0.2NA | |
| C. | 7.8gNa2O2和Na2S的混合物中含有的离子总数为0.7NA | |
| D. | 常温下,1L0.1mol/LNa2CO3溶液中,含有离子的总数大于0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯分子有7个σ键,1个π键 | |
| B. | 丙烯分子中3个碳原子都是sp2杂化 | |
| C. | 丙烯分子中最多有7个原子共平面 | |
| D. | 丙烯分子中3个碳原子在同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
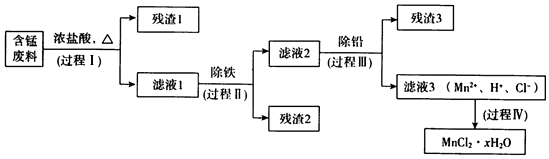
| Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 8.1 | 6.5 | 1.9 |
| 完全沉淀时 | 10.1 | 8.5 | 3.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
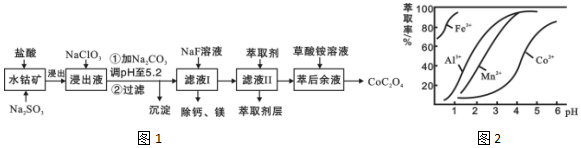
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com