
| A. | ①②③ | B. | ①④ | C. | ①③ | D. | ①②③④ |
分析 中学常见既能跟盐酸反应,又能跟氢氧化钠溶液反应的物质有:Al、Al2O3、Al(OH)3、弱酸的酸式盐、弱酸的铵盐、蛋白质、氨基酸等.
解答 解:①Al与盐酸反应生成氯化铝与氢气,与氢氧化钠溶液反应生成偏铝酸钠与氢气,故①正确;
②Al2O3属于两性氧化物,与盐酸反应生成氯化铝与水,与氢氧化钠溶液反应生成偏铝酸钠与水,故②正确;
③Al(OH)3属于两性氢氧化物,与盐酸反应生成氯化铝与水,与NaOH溶液反应生成偏铝酸钠与水,没有气体生成,故③正确;
④NaHCO3溶液能与盐酸反应生成二氧化碳气体,与氢氧化钠反应生成碳酸钠,故④正确;
故选D.
点评 本题考查元素化合物的性质,难度不大,关键是对物质性质的掌握,注意归纳总结常见能与酸、碱反应的物质.


科目:高中化学 来源: 题型:选择题
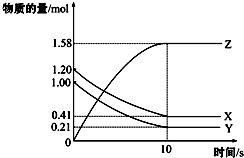
| A. | 反应开始到10s,用Z表示的反应速率为0.079mol/(L•s) | |
| B. | 该反应的方程式为:X(g)+Y(g)?2 Z(g) | |
| C. | 反应开始到10s时,Y的转化率为79.0% | |
| D. | 反应进行到10s时,该反应达到限度且各组分浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用过量氨水除去Al3+溶液中的少量Fe3+ | |
| B. | 将混合气体通过灼热的铜网除去N2中的少量O2 | |
| C. | 用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 | |
| D. | 用饱和NaHCO3溶液除去混在H2中的HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
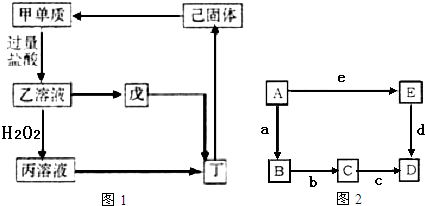
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
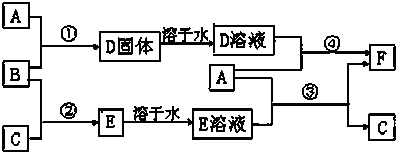
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体 | |
| B. | 加热蒸发K2CO3溶液获得K2CO3晶体 | |
| C. | 加热蒸发FeCl2溶液制取Fe(OH)2固体 | |
| D. | 加热蒸发MgCl2溶液制取MgCl2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
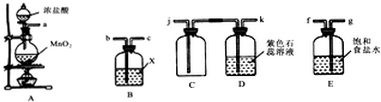
| 实验装置设计. | 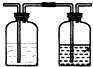 (注明所用试剂及气体流向) (注明所用试剂及气体流向)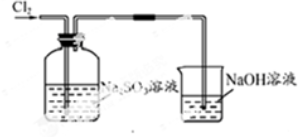 |
| 实验步驟及现象 | 连接好装置,将氯气通入亚硫酸钠溶液中,充分反应.取少量所得溶液与试管,滴入几滴氯化钡,有白色沉淀,再加入少量盐酸,沉淀不溶解. |
| 离子方程式 | Cl2+SO32-+H2O=2Cl-+SO42-+2H+; SO42-+Ba2+=BaSO4↓ |
| 结论 | Na2SO3具有还原性,能被氯气氧化成Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 光照甲烷和氯气的混合气体 | B. | 苯在镍催化作用下与氢气发生反应 | ||
| C. | 乙醇与酸性高锰酸钾溶液的反应 | D. | 苯和液溴混合加入铁粉的反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com