
在一定温度下,饱和氯水中存在平衡:Cl2+H2O H++Cl-+HClO。下列说法中确的是
H++Cl-+HClO。下列说法中确的是
A.光照一段时间后,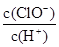 增大 增大 |
| B.加入碳酸钙粉末后,溶液的pH增大 |
| C.加入少量水,由水电离的c(H+)减小 |
| D.加入NaOH固体,一定有c(Na+)>c(Cl-)>c(H+)>c(ClO-)) |
B
解析试题分析:A、次氯酸不稳定,光照HClO易分解生成HCl和氧气,所以溶液中c(ClO-)降低,c(H+)增大,因此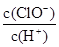 减小,故A错误;B、碳酸的酸性强于次氯酸的,所以碳酸钙与次氯酸不反应,而与盐酸反应,虽然平衡向正反应移动,但溶液中c(H+)仍然是减小的,因此溶液的pH增大,故B正确;C、稀释溶液,溶液中c(H+)减小,c(OH-)浓度增大,溶液中OH-的浓度等于水电离的H+的浓度,因此水电离的c(H+)增大,故C错误;D、如果加入过量的氢氧化钠,则溶液中c(ClO-)远远大于c(H+),故D错误,答案选B。
减小,故A错误;B、碳酸的酸性强于次氯酸的,所以碳酸钙与次氯酸不反应,而与盐酸反应,虽然平衡向正反应移动,但溶液中c(H+)仍然是减小的,因此溶液的pH增大,故B正确;C、稀释溶液,溶液中c(H+)减小,c(OH-)浓度增大,溶液中OH-的浓度等于水电离的H+的浓度,因此水电离的c(H+)增大,故C错误;D、如果加入过量的氢氧化钠,则溶液中c(ClO-)远远大于c(H+),故D错误,答案选B。
考点:考查外界条件对平衡状态的影响;溶液酸碱性以及溶液中离子浓度大小比较等


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:单选题
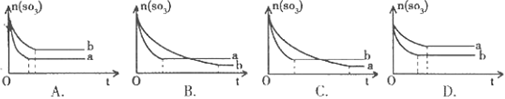
一定温度下,往a、b两容器中各注人1 mol三氧化硫,a、b两容器起始体积和压强均相同,分别保持恒容和恒压,发生以下反应: 2SO3(g) 2SO2(g)+O2(g),两容器中三氧化硫物质的量随时间(t)变化的示意图为
2SO2(g)+O2(g),两容器中三氧化硫物质的量随时间(t)变化的示意图为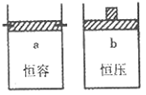
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于反应N2(g)+3H2(g) 2NH3(g) △H=-92kJ/mol,若只改变下列一个条件,一定能增大正反应速率且使平衡向正反应方向移动的是( )
2NH3(g) △H=-92kJ/mol,若只改变下列一个条件,一定能增大正反应速率且使平衡向正反应方向移动的是( )
| A.升高温度 | B.增大容器体积 |
| C.降低c(NH3) | D.将三种物质浓度均增大到原来的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在密闭容器中进行反应:A(g)+3B(g) 2C(g),有关下列图像说法的不正确的是
2C(g),有关下列图像说法的不正确的是
| A.依据图a可判断正反应为放热反应 |
| B.在图b中,虚线可表示使用了催化剂 |
| C.若正反应的△H<0,图c可表示升高温度使平衡向逆反应方向移动 |
| D.由图d中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实不能用勒夏特列原理解释的是
| A.配制氯化铁溶液时,加入少量稀盐酸 |
| B.配制氯化亚铁溶液时,加入少量铁屑 |
| C.在含有酚酞的氨水中加入少量NH4Cl,溶液颜色会变浅 |
| D.在硫酸铜饱和溶液中加入一块胆矾,晶体外形变规则 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度下的密闭容器中发生反应:X(g)+3Y(g) 2Z(g) △H<
2Z(g) △H< ,如图是反应达平衡及改变条件平衡移动的图像。下列说法错误的是
,如图是反应达平衡及改变条件平衡移动的图像。下列说法错误的是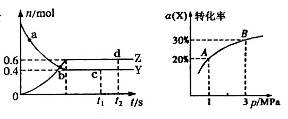
A.c点和d点X的正逆反应速率相等
B.起始时,加入Y的物质的量为1.3mol
C.平衡状态由A变到B时,平衡常数:K(A)<K(B)
D.平衡状态由A变到B时,放出的热量:Q(A)<Q(B)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g) +H2O(g)=CO(g) +3H2(g) △H>0,在一定条件下,向体积为1L的密闭容器中充入1 mol CH4(g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是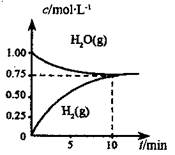
| A.达平衡时,CH4( g)的转化率为75% |
| B.0~10 min 内,v(CO)=0.075 mol?L-1·min-1 |
| C.该反应的化学平衡常数K=0.1875 mol?L-1 |
| D.当CH4(g)的消耗速率与H2O(g)的生成速率相等,反应到达平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
2NH3(g) △H=-92.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
| A.前20分钟反应内放出的热量为46.2kJ |
| B.第25分钟改变的条件是将NH3从反应体系中分离出去 |
| C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
aZ(g) △H=QkJ·mol-1,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图像,下列有关说法正确的是
| A.图甲,P1>P2,a < 3 |
| B.图甲,T1<T2,Q>0 |
| C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体 |
| D.图乙,如果a=3, t2时表示向体系中加入了催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com