
分析 根据n=$\frac{m}{M}$计算氨基酸的物质的量,由消耗氢氧化钠可以确定-COOH数目,再计算去掉羧基、H原子后氨基酸中剩余碳原子和氮原子式量之和,进而确定C、N原子数目,是天然蛋白质的水解产物,则氨基、羧基连接同一碳原子上.
解答 解:氨基酸的物质的量=$\frac{0.318g}{147g/mol}$,
n(NaOH)=0.0216L×0.2mol/L=0.00432mol,
因为氨基酸和NaOH物质的量比$\frac{0.318g}{147g/mol}$:0.00432=1:2,所以氨基酸分子中有2个羧基,
去掉羧基、H原子后氨基酸中剩余碳原子和氮原子式量之和为147-45×2-(9-2)=50,即为C3N,
由于是天然蛋白质的水解产物,所以氨基酸为: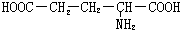 ,
,
答:该氨基酸的结构简式为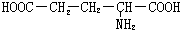 .
.
点评 本题考查有机物推断,属于计算型推断,关键是确定羧基数目,注意残余法的应用,难度不大.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径A<B<C | |
| B. | A与C可形成离子化合物 | |
| C. | A的氧化物熔点比B的氧化物高 | |
| D. | B单质可与A的最高价氧化物发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NH3+3Cl2═N2+6HCl | B. | 2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$ N2+3Cu+3H2O | ||
| C. | Cl2+2NaOH═NaCl+NaClO+H2O | D. | KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | A | B | C | D | E | F |
| 原子半径/nm | 0.186 | 0.143 | 0.160 | 0.102 | 0.074 | 0.099 |
| 主要化合价 | +l | +3 | +2 | +6、-2 | -2 | +7、-1 |
| A. | 元素D位于第三周期Ⅵ族 | |
| B. | A、B、C三种元素的最高价氧化物对应水化物的碱性依次增强 | |
| C. | 1mol F的单质参加氧化还原反应时转移的电子数一定为2 mol | |
| D. | 元素B、E形成的化合物具有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中碳碳键是介于C-C和C=C之间的一种特殊共价键 | |
| B. | 甲烷、乙烯都能使酸性KMnO4溶液褪色 | |
| C. | 葡萄糖溶液中加入银氨溶液,水浴加热有银镜生成 | |
| D. | 医用酒精能使蛋白质变性,可用于消毒杀菌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com