
���� ��1������C=$\frac{1000�Ѧ�}{M}$����Ũ��������ʵ���Ũ�ȣ�����ϡ��ǰ�����ʵ����ʵ������������ҪŨ����������
��2����������һ�����ʵ���Ũ����Һ��һ�㲽��ȷ��ʹ��������
��3���������������ʵ����ʵ�������Һ�����Ӱ�죬����C=$\frac{n}{V}$������������
��� �⣺��1��98%���ܶ�Ϊ1.84g•cm-3����Ũ��������ʵ���Ũ��C=$\frac{1000��1.84��98%}{98}$=18.4mol/L������240mL1.0mol•L-1ϡ���ᣬʵ����û��240mL����ƿ��Ӧѡ��250mL����ƿ��ʵ������250mL��Һ������ҪŨ�������ΪV������ϡ��ǰ�����ʵ����ʵ����������ã�V��18.4mol/L=1mol•L-1��250mL�����V=13.6mL��
�ʴ�Ϊ��13.6��
��2����Ũ��Һ����һ�����ʵ���Ũ��ϡ��Һһ�㲽��Ϊ�����㡢��ȡ��ϡ�͡���ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȣ��õ��������У���Ͳ�����������ձ���250mL����ƿ����ͷ�ιܣ�����Ҫ������Ϊ��250 mL����ƿ����ͷ�ιܣ�
�ʴ�Ϊ��250 mL����ƿ����ͷ�ιܣ�
��3���ٳ���ʱ��������ƽ���̼����룬���̼��Ȼ��ƣ�������ƽ����ԭ�������ʵ�����=���������-���������������ʵ�ʳ����Ĺ�������ƫС�����ʵ����ʵ���ƫС����ҺŨ��ƫ�ͣ��ʲ�ѡ��
������ƿʹ��ʱδ��������ʵ����ʵ�������Һ������������Ӱ�죬��ҺŨ����Ӱ�죬�ʲ�ѡ��
�۶��ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶��ߣ�������Һ���ƫ����ҺŨ��ƫ�ͣ��ʲ�ѡ��
����Һ��δϴ���ձ��Ͳ��������������ʵ����ʵ���ƫС����ҺŨ��ƫС���ʲ�ѡ��
�ݶ���ʱ���ӿ̶��߹۲�Һ�棬������Һ���ƫС����ҺŨ��ƫ�ߣ���ѡ��
��ѡ���ݣ�
���� ���⿼��������һ�������ٷ���Ũ�Ⱥ�һ�����ʵ���Ũ����Һ����ȷ���õ�ԭ������ȷ�IJ��������ǽ���ؼ������ؿ���ѧ���Ի���ʵ��ԭ���Ͳ����������������Ŀ�ѶȲ���


 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �������ͼװ�ûش�
�������ͼװ�ûش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NO | B�� | NO2 | C�� | N2O | D�� | N2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ˮ������Ӧ���ɱ���Ĥ��2Fe+6H2O��g���T2Fe��OH��3+3H2 | |
| B�� | �����Ƶ������������м���������ϡ���Fe��OH��2+2H+�TFe2++2H2O | |
| C�� | ʢ������������Һ���Լ�ƿ�����ò�������SiO2+2OH-�TSiO32-+H2O | |
| D�� | ���Ȼ�����Һ�м������������������Һ��Al3++3OH-�TAl��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���������� | ʵ��Ŀ�� |
| A | �����������Թ��У��������û | ��֤����������ʴ |
| B | ��NaBr��Һ�е���������ˮ�ͱ��������ã���Һ�ϲ�ʳȺ�ɫ | ֤��Br-��ԭ��ǿ��Cl- |
| C | ���Ȼ���������������������ˮ�� | ����FeCl2��Һ |
| D | �������Ȼ������ʵ�����ͨ��װ�б���NaHCO3��Һ��ϴ��ƿ | ��ȥ�����е�HCl���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | CO��N2Ϊ�ȵ����壬22.4 L��CO������l mol N2�����ĵ�������� | |
| B�� | ��2.4 gʯī�У���C-C���ۼ���ĿΪ0.3NA | |
| C�� | 720 g C60���庬��0.25NA��������������ͼ�� | |
| D�� | 1mol[Cu��NH3��4]2+�к���λ��4 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �۵�� | B�� | �ܶ�С | C�� | Ӳ��С | D�� | ��ѧ���ʻ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.3 g Na��O2��ȫ��Ӧ����3.6 g����ʱʧ��������0.1��6.02��1023�� | |
| B�� | ��1 mol FeCl3��FeCl3������Һ��ȫ��Ӧ��������1mol Fe��OH��3�������� | |
| C�� | 11.2L������̼�����������ķ�����Ϊ0.5NA | |
| D�� | �����Ϲ涨��0.012kg̼ԭ�������е�̼ԭ����ĿΪ1mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
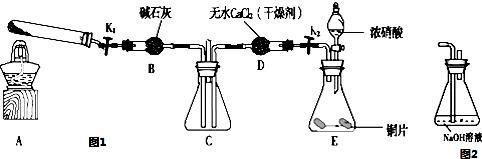
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com