
| A. | C6H13COOH | B. | C6H5COOH | C. | C7H15COOH | D. | C6H5CH2COOH |
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl2是一种黄绿色的有毒气体 | B. | 红热的铁丝在Cl2中燃烧生成FeCl2 | ||
| C. | 工业上用Cl2和石灰乳制造溧白粉 | D. | 新制氯水应避光保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减压时,v(逆)增大,v(正)减小,平衡向逆反应方向移动 | |
| B. | 若加入2a mol HI,则平衡常数变为2倍 | |
| C. | 加压时,v(逆)、v(正)均不变,平衡不移动 | |
| D. | 若保持压强不变,通入氦气,则v(逆)、v(正)均减小,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①②③④⑤⑥⑦ | B. | ②③④⑤⑥ | C. | ②③④⑤⑥⑦ | D. | ①②③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X、W的简单阴离子具有相同的电子层结构 | |
| B. | 原子半径:r(Y)<r(X)<r(W)<r(Z) | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | 由X、Z两种元素组成的化合物是离子化合物,只含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
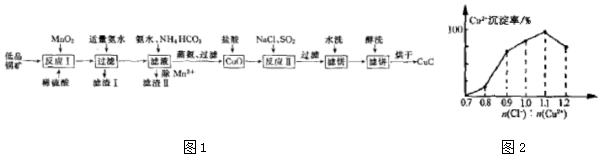
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量 | |
| B. | △H1=△H3>△H2 | |
| C. | △H1<△H3 | |
| D. | 28gCO的能量比44gCO2的能量高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com