
【题目】下列有关化学用语正确的是( )
A. 某元素基态原子的电子排布图![]()
B. NH4Cl电子式为[![]() :H]+Cl-
:H]+Cl-
C. Ca2+基态电子排布式为1s22s22p63s23p6
D. α羟基丙酸(乳酸)的比例模型为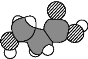
科目:高中化学 来源: 题型:
【题目】如图是硫酸试剂瓶标签上的部分内容。据此下列说法中正确的是( )
硫酸 化学纯CP
500 mL
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84 g·cm-3
质量分数:98%
A.该硫酸可以用来干燥硫化氢气体
B.1molZn与足量的该硫酸反应能产生2gH2
C.配制250mL4.6mol·L-1的稀硫酸需取该硫酸62.5mL
D.若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100.0 mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到16.84g沉淀,用过量稀硝酸处理后沉淀质量减少至6.99g,同时溶液中有气泡产生。试求:
(1)原混合液中Na2SO4的物质的量浓度为_____;
(2)产生的气体在标准状况下的体积为多少__________?(要求写出计算过程,只写结果不给分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是重要的化工产品,在基础化学试验中,有着重要的作用。
(1)质量分数为98%(密度1.84 g/cm3)的浓硫酸在实验室中常用作吸水剂,其物质的量浓度为_________。
(2)若用上述质量分数为98%的硫酸,配制480 mL物质的量浓度为2.3 mol/L的硫酸,所需浓硫酸的体积为_________ mL。
(3)取用任意体积的浓硫酸时,下列物理量中不变的是_________。
A.溶液中H2SO4的物质的量 B.溶液的浓度 C.溶液的质量 D.溶液的密度
(4)完成(2)中实验除了烧杯、量筒、玻璃棒外,还需要的仪器有_________。
(5)下列操作使所配溶液的物质的量浓度偏高的_________(填序号)。
A.用量筒量取浓H2SO4,慢慢地沿着玻璃棒注入盛有50 mL蒸馏水的小烧杯,搅拌后,立即转移到容量瓶中
B.往容量瓶转移溶液时,有少量液体溅出
C.未洗涤稀释浓H2SO4的小烧杯
D.定容时俯视
E.容量瓶未干燥即用来配制溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(![]() )是一种清洁能源,可由合成气(
)是一种清洁能源,可由合成气(![]() 、
、![]() )来制备,反应原理如下:
)来制备,反应原理如下:
反应Ⅰ:![]()
![]()
反应Ⅱ:![]()
![]()
回答下列问题:
(1)上述反应符合“原子经济性”原则的是__________(填“反应Ⅰ”或“反应Ⅱ”)。
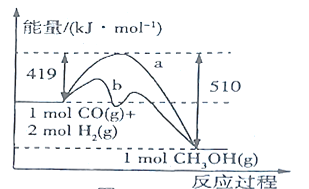
(2)图中使曲线![]() 对应反应按曲线
对应反应按曲线![]() 进行的措施是__________,由合成气(
进行的措施是__________,由合成气(![]() 、
、![]() )制备
)制备![]() 的热化学方程式为__________,该反应自发进行的条件为_________(填“低温”或“高温”)。
的热化学方程式为__________,该反应自发进行的条件为_________(填“低温”或“高温”)。
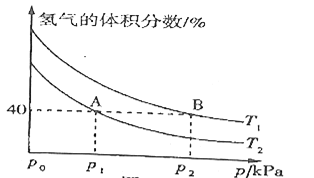
(3)模拟该制备原理,起始时在某容器中充入![]() 和
和![]() 合成
合成![]() ,平衡时混合物中氢气的体积分数与温度、压强的关系如图所示:
,平衡时混合物中氢气的体积分数与温度、压强的关系如图所示:
①下列有关说法能够证明恒温恒压时,反应![]()
![]() 一定达到平衡状态的是__________(填序号)。
一定达到平衡状态的是__________(填序号)。
![]() .
.![]() 和
和![]() 的转化率相等
的转化率相等
![]() .反应体系中混合气体密度保持不变
.反应体系中混合气体密度保持不变
![]() .
.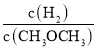 的值保持不变
的值保持不变
![]() .反应体系压强保持不变
.反应体系压强保持不变
②图中![]() ________
________![]() (填“>”“<”或“=”);理由是____________。
(填“>”“<”或“=”);理由是____________。
③在![]() 、
、![]() 两点对应的条件下,该反应从开始到平衡时生成二甲醚的平均速率:
两点对应的条件下,该反应从开始到平衡时生成二甲醚的平均速率:![]() _____
_____![]() 。
。
④![]() 点对应的
点对应的![]() _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸是一种绿色生态杀菌剂,结构简式为 ,可用乙酸与过氧化氢一定条件下反应制得。下列说法不正确的是( )
,可用乙酸与过氧化氢一定条件下反应制得。下列说法不正确的是( )
A.过氧化氢的电子式![]()
B.乙酸溶于水:CH3COOH=CH3COO-+H+
C.过氧乙酸中含有极性共价键和非极性共价键
D.制备过氧乙酸的化学反应方程式:CH3COOH+H2O2![]() CH3COOOH+H2O
CH3COOOH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列用于解释事实的离子方程式不正确的是( )
A.向AgCl悬浊液中加入Na2S溶液,有黑色难溶物生成:2AgCl(s)+S2-(aq)![]() Ag2S(s)+2Cl-(aq)
Ag2S(s)+2Cl-(aq)
B.向酸性KMnO4溶液中加入NaHSO3固体,溶液紫色褪去:2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O
C.向NaHCO3溶液中加入过量澄清石灰水,有白色沉淀生成:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32-
D.向稀硝酸中加入铜粉,溶液变蓝色:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的现象与结论相对应的是( )
A | B | C | D | |
实验 |
|
|
|
|
现象 | 一段时间后,a管液面高于b管液面 | 酸性KMnO4溶液褪色 | pH计测得①中pH大于②中pH | 试管①中有大量气泡,试管②中无现象 |
结论 | a管发生吸氧腐蚀,b管发生析氢腐蚀 | 有乙烯生成可以使酸性KMnO4溶液褪色 | 金属性:Mg>Al | 酸性:醋酸>碳酸>硼酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两个相同带活塞的容器,向容器a中充入NO2(g)待颜色不再变化,再向容器b中充入溴蒸汽,使两容器的颜色和体积相等〔注意:同浓度的NO2和Br2蒸汽颜色相同,2NO2(g)![]() N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
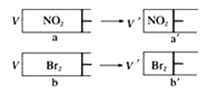
A.a→a′过程中,颜色突然加深,然后逐渐变浅,最终颜色比原来的浅
B.若对a和b以极慢的速度缓缓压缩,则a和b的颜色均慢慢加深,但在每一个相同的时间点,b的颜色总比a的深
C.假设容器和活塞均为无色,从容器左侧观察a和a′,a′的颜色比a浅
D.气体的物质的量:na一定大于nb′
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com