
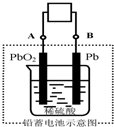
 电瓶车所用的电池一般是铅蓄电池,该电池电压稳定,安全可靠,价格低廉,在生产、生活中广泛使用.其电池总反应式为:
电瓶车所用的电池一般是铅蓄电池,该电池电压稳定,安全可靠,价格低廉,在生产、生活中广泛使用.其电池总反应式为:| 放电 |
| 充电 |
| 1mol |
| 2 |


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:

| A、该检测装置实现了将化学能转化为电能,且单位时间内通过电量越大,酒精含量越高 |
| B、电极A是正极 |
| C、电极B的反应:H2O+C2H5OH-4e-=CH3COOH+4H+ |
| D、电池总反应:O2+C2H5OH=CH3COOH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电子将沿着Zn→a→b→Cu路径流动 |
| B、片刻后可观察到试纸a点变蓝色 |
| C、反应一段时间,乙池溶液浓度上升 |
| D、锌电极上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 四川盛产五倍子.以五倍子为原料可以制得化合物A.A的结构简式如图所示:请回答下列问题:
四川盛产五倍子.以五倍子为原料可以制得化合物A.A的结构简式如图所示:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| Cu或Ag |
 .请推断乳酸的结构简式:
.请推断乳酸的结构简式:查看答案和解析>>
科目:高中化学 来源: 题型:
A、用惰性电极电解熔融氯化钠:2Cl-+2H2O
| ||||
| B、用稀硫酸溶液除去铜表面的氧化铜:CuO+2H+=Cu2++H2O | ||||
| C、常温下,用稀氢氧化钠溶液吸收多余的氯气:Cl2+OH-=Cl-+ClO-+H2O | ||||
| D、苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 150℃ |
| 催化剂 |
| A、平衡时,其他条件不变,升高温度可使该反应的速率加快,平衡常数增大 |
| B、平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C、平衡时,其他条件不变,增大压强,废气中氮氧化物的转化率减小 |
| D、平衡时,其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com