
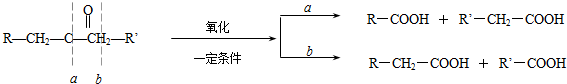
 )生成一种合成纤维:
)生成一种合成纤维: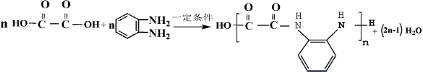 .
.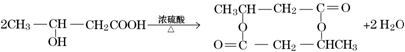 .
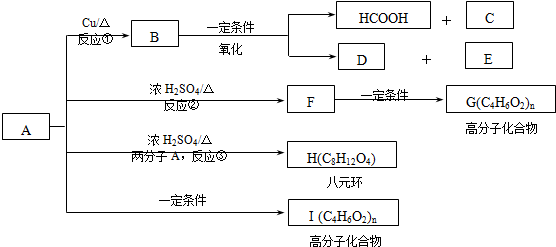
.分析 A在浓硫酸、加热作用下生成F,F可以形成高聚物G,且F可使溴水褪色,结合G的分子式可知,F分子中含有C=C,且其中含甲基,根据G可知F为CH3CH=CHCOOH,G为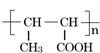 ,根据A发生氧化反应得到B,B可以发生信息中的反应,则A分子中存在-OH,结合F可知A分子中含有-COOH,则A应为CH3-CH(OH)-CH2-COOH,氧化生成B为
,根据A发生氧化反应得到B,B可以发生信息中的反应,则A分子中存在-OH,结合F可知A分子中含有-COOH,则A应为CH3-CH(OH)-CH2-COOH,氧化生成B为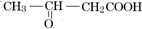 ,则C为HOOC-CH2-COOH,D的相对分子质量比E小,结合题给信息可知D为CH3COOH,E为HOOC-COOH,由A与H的分子式可知,A脱去2分子水形成H为八元环的环酯,H为
,则C为HOOC-CH2-COOH,D的相对分子质量比E小,结合题给信息可知D为CH3COOH,E为HOOC-COOH,由A与H的分子式可知,A脱去2分子水形成H为八元环的环酯,H为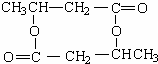 ,A发生缩聚反应生成高分子化合物I,据此解答.
,A发生缩聚反应生成高分子化合物I,据此解答.
解答 解:A在浓硫酸、加热作用下生成F,F可以形成高聚物G,且F可使溴水褪色,结合G的分子式可知,F分子中含有C=C,且其中含甲基,根据G可知F为CH3CH=CHCOOH,G为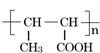 ,根据A发生氧化反应得到B,B可以发生信息中的反应,则A分子中存在-OH,结合F可知A分子中含有-COOH,则A应为CH3-CH(OH)-CH2-COOH,氧化生成B为
,根据A发生氧化反应得到B,B可以发生信息中的反应,则A分子中存在-OH,结合F可知A分子中含有-COOH,则A应为CH3-CH(OH)-CH2-COOH,氧化生成B为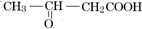 ,则C为HOOC-CH2-COOH,D的相对分子质量比E小,结合题给信息可知D为CH3COOH,E为HOOC-COOH,由A与H的分子式可知,A脱去2分子水形成H为八元环的环酯,H为
,则C为HOOC-CH2-COOH,D的相对分子质量比E小,结合题给信息可知D为CH3COOH,E为HOOC-COOH,由A与H的分子式可知,A脱去2分子水形成H为八元环的环酯,H为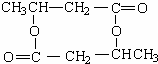 ,A发生缩聚反应生成高分子化合物I,
,A发生缩聚反应生成高分子化合物I,
(1)由以上分析可知A为CH3-CH(OH)-CH2-COOH,A中具有的官能团为羟基和羧基,
故答案为:羟基和羧基;
(2)由以上分析可知,C为HOOC-CH2-COOH,D为CH3COOH,
故答案为:HOOC-CH2-COOH;CH3COOH;
(3)反应①为CH3-CH(OH)-CH2-COOH的催化氧化,反应②CH3-CH(OH)-CH2-COOH在浓硫酸作用下发生消去反应的过程,
故答案为:氧化;消去;
(4)G为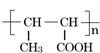 ,含有羧基,能与氢氧化钠溶液发生中和反应,与甲醇发生酯化反应,不能与溴或高锰酸钾溶液反应,故选ad;
,含有羧基,能与氢氧化钠溶液发生中和反应,与甲醇发生酯化反应,不能与溴或高锰酸钾溶液反应,故选ad;
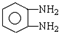
(5)(1)E为HOOC-COOH,与邻苯二胺(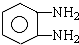 )缩聚生成一种合成纤维方程式为:
)缩聚生成一种合成纤维方程式为: ,
,
(2)A为CH3-CH(OH)-CH2-COOH,两分子A可发生酯化反应生成环,反应的方程式为 ,
,
故答案为: ;
; ;
;
(6)反应②为CH3-CH(OH)-CH2-COOH的消去反应,可能生成副产物为CH2=CHCH2COOH,
故答案为:CH2=CHCH2COOH.
点评 本题考查有机物的推断,题目难度较大,本题注意以F为突破口进行推断,同时注意题给信息,为解答该题的关键,难度不大.


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:多选题
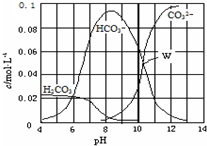
| A. | W点所示的溶液:c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) | |
| B. | pH=4的溶液:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1 mol•L-1 | |
| C. | 向pH=8的溶液中通入CO2至pH=7所得的溶液:c(Na+)>c(Cl-)+c(HCO3-)+c(H2CO3) | |
| D. | pH=11的溶液:c(Na+)+2c(H2CO3)>2c(Cl-)+2c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 弱碱的浓度大于强酸的浓度 | |
| B. | 原氨水中有1%的含氮微粒为NH4+ | |
| C. | 反应后的溶液呈酸性 | |
| D. | 混合溶液中c(NH4+)+c(NH3•H2O)+c(NH3)=5×10-4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数相等,质量不相等 | B. | 质子数、质量都不相等 | ||
| C. | 分子数、质量分别相等 | D. | 原子数、电子数都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.
图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16.5g | B. | 85g•mol-1 | C. | 65 g | D. | 55g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的结构式:H-Cl-O | |
| B. | 含有10个中子的氧原子的符号:${\;}_{8}^{18}$O | |
| C. | S2-的结构示意图 | |
| D. | NH4Cl的电子式: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com