
 Ti��Fe��Cu��NiΪ���ɽ���Ԫ�أ��ڹ�ҵ����������Ҫ��Ӧ�ã�
Ti��Fe��Cu��NiΪ���ɽ���Ԫ�أ��ڹ�ҵ����������Ҫ��Ӧ�ã����� ��1����Fe��CO��5�۷е�Ƚϵͣ����Ϸ��Ӿ������ʣ�Fe��CO֮���γ���λ����CO�д��ڼ��Լ���
��������[Fe��NO����H2O��5]2+��Fe2+���������ӣ�NO��H2O�����壻H2O��Oԭ���γ�2��O-H��������2�Թ¶Ե��ӣ��ӻ������ĿΪ4��
�����ӵ����ͬ�����Ӱ뾶ԽС��������Խ�����Ӿ�����۷е�Խ�ߣ�
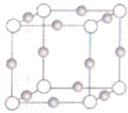
��2�����ڵİ��������֮��ľ���Ϊa cm�����ⳤΪ2a cm�����ݾ�̯�����㾧����Cu��Nԭ����Ŀ����ʾ�������������ٸ��ݦ�=$\frac{m}{V}$���㾧���ܶȣ�
��� �⣺��1���ٳ�����Fe��CO��5��Һ̬���۵�Ϊ-20.5�棬�е�Ϊ103�棬���Ϸ��Ӿ������ʣ�Ӧʹ�÷��Ӿ��壻Fe��CO֮���γ���λ����CO�д��ڼ��Լ���
�ʴ�Ϊ�����Ӿ��壻BD��
��������[Fe��NO����H2O��5]2+��Fe2+���������ӣ�NO��H2O�����壬Fe2+����λ��Ϊ6��H2O��Oԭ���γ�2��O-H��������2�Թ¶Ե��ӣ��ӻ������ĿΪ4��Oԭ�Ӳ�ȡsp3�ӻ���
�ʴ�Ϊ��6��sp3�ӻ���
��NiO��FeO�ľ���ṹ���;��������Ƶ���ͬ�����������Ӿ��壬���ӵ����ȣ������Ӱ뾶Ni2+��Fe2+����NiO�ľ����ܴ���FeO�ģ����۵�NiO��FeO��
�ʴ�Ϊ������
��2�����ڵİ��������֮��ľ���Ϊa cm�����ⳤΪ2a cm��������Cuԭ����ĿΪ12��$\frac{1}{4}$=3��Nԭ����Ŀ=8��$\frac{1}{8}$=1��������Ϊ$\frac{64��3+14}{{N}_{A}}$g�����ܶ�Ϊ$\frac{64��3+14}{{N}_{A}}$g�£�2a cm��3=$\frac{103}{4{a}^{3}•{N}_{A}}$g•cm-3��
�ʴ�Ϊ��$\frac{103}{4{a}^{3}•{N}_{A}}$��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰�������������ʡ���ѧ���������ӻ���ʽ���۷е�Ƚϡ���������ȣ����վ�̯�����о����йؼ��㣮


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������KI��Һ����������ɫ | |
| B�� | ���ۺ���ά�����ڶ��ǣ������ʽ��Ϊ��C6H10O5��n������Ϊͬ���칹�� | |
| C�� | ����һ�㲻����ˮ��û����ζ��û�л�ԭ�� | |
| D�� | ��ϡ���������£�����ˮ�����������Ǻ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2��g��+O2��g��?2NO��g����H=+181.5kJ/mol | |
| B�� | NH3��ȼ����Ϊ226.25kJ/mol | |
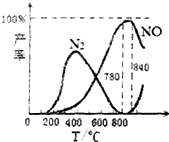
| C�� | ��ҵ�ϰ�����������NOʱ���¶�Ӧ������780��840��֮�� | |
| D�� | �ò�˿�����������÷�Ӧ�����Ʊ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H5OH��l��+3O2��g���T2CO2��g��+3H2O��g����H=-1 367.0 kJ•mol-1��ȼ���ȣ� | |
| B�� | KOH��aq��+HNO3��aq���TKNO3+H2O��l����H=+57.3 kJ•mol-1���к��ȣ� | |
| C�� | S��s��+O2��g���TSO2��g����H=-269.8 kJ•mol-1����Ӧ�ȣ� | |
| D�� | 2NO2�TO2+2NO��H=+116.2 kJ•mol-1����Ӧ�ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2ʹƷ�졢���Ը��������Һ��ɫ���ֱ�����������Ư���Ժͻ�ԭ�� | |
| B�� | ��Fe��NO3��2��Ʒ����ϡH2SO4�μ�KSCN��Һ����Һ��죬˵��Fe��NO3��2��Ʒ�Ѿ����� | |
| C�� | ��δ֪��Һ�еμ�BaCl2��Һ���ְ�ɫ������������������ܽ⣬˵������Һһ������SO42- | |
| D�� | Ũ��������ڸ���H2��NO2�����壬�����ܸ���NH3��SO2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 +Br2��
+Br2�� ����Ӧ�����Ǽӳɷ�Ӧ��
����Ӧ�����Ǽӳɷ�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 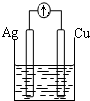 ϡ���� | B�� | 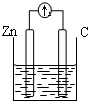 AgNO3��aq�� | C�� | 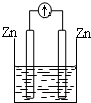 ���� | D�� | 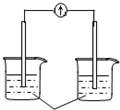 ϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6A% | B�� | 10A% | C�� | $\frac{A}{6}$% | D�� | ��100-$\frac{7A}{6}$��% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com