
| A. | N2(g)+3H2(g)?2NH3(g) (正反应为放热反应) | |
| B. | C(s)+CO2(g)?2CO(g) (正反应为吸热反应) | |
| C. | 2NO2(g)?N2O4(g) (正反应为放热反应) | |
| D. | 3O2(g)?2O3(g) (正反应为吸热反应) |
科目:高中化学 来源: 题型:选择题
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 鉴别己烯和苯:分别向己烯和苯中滴入酸性KMnO4溶液,振荡,观察是否褪色 | |
| C. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| D. | 检验卤代烃中的卤素原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
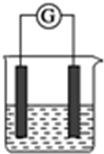 选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、Fe、Cu、Zn,组成右图所示的原电池装置(只有两个电极),观察到电流计?的指针均明显转偏,则其可能的组合共有( )
选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、Fe、Cu、Zn,组成右图所示的原电池装置(只有两个电极),观察到电流计?的指针均明显转偏,则其可能的组合共有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验方法 | |
| A | 检验某混合溶液中是否有Cl- | 取样滴加AgNO3溶液 |
| B | 除去食盐中的少量氯化铵 | 加热 |
| C | 鉴别CO2和SO2 | 分别通入澄清石灰水 |
| D | 证明某地雨水样品呈酸性 | 取样滴入酚酞 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘水 | B. | 碘水、烧碱溶液、新制的Cu(OH)2 | ||
| C. | 氢氧化钠溶液、银氨溶液 | D. | 烧碱溶液、新制的Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤ | C. | ①③⑥ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径:W>Y>Z>X | |
| B. | 气态氢化物的稳定性:X>Z | |
| C. | Y、Z的氧化物都有两性 | |
| D. | 最高价氧化物对应水化物的碱性:Y>W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com