
【题目】2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰,表彰他们对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
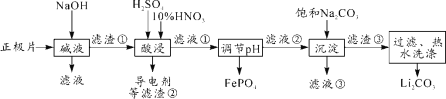
(1)从“正极”可以回收的金属有___________。
(2)“碱溶”时Al箔溶解的离子方程式_________。
(3)“酸浸”时产生标准状况下2.24L NO时,则被氧化的LiFePO4为______mol。(其他杂质不与HNO3反应)
(4)实验测得滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,Li+的沉降率到99%,则滤液③中c(CO32-)=________ mol·L-1。 [Ksp(Li2CO3)=1.6×10-3]
(5)磷酸亚铁锂电池总反应为:LiFePO4+6C ![]() Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向_______(填“阳极”或“阴极”);放电时,正极反应式为_______。
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向_______(填“阳极”或“阴极”);放电时,正极反应式为_______。
(6)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取1.40g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030 mol·L-1重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00mL。
已知:2Fe3++Sn2++6Cl-=SnCl62-+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
① 实验中加入HgCl2饱和溶液的目的是__________。
② 磷酸亚铁锂电池中铁的含量为_______。
【答案】Li、Fe、Al 2Al+2OH-+2H2O=2AlO2-+3H2↑ 0.3 4 阴极 Li1-xFePO4+xLi++xe-=LiFePO4 将溶液中过量Sn2+转化为稳定的SnCl62-,防止其干扰Fe2+的测定 28.8%
【解析】
(1)根据分析流程,碱溶可得到NaAlO2滤液,调节pH值,生成的沉淀为FePO4,加入碳酸钠,可生成Li2CO3沉淀,因此从“正极”可以回收的金属有Li、Fe、Al,故答案为:Li、Fe、Al;
(2)碱溶时Al箔与氢氧化钠反应,溶解的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)酸浸时HNO3转化为NO,产生标准状况下2.24LNO的物质的量为![]() =0.1mol,产生1molNO,转移3mol电子,则生成0.1molNO转移0.3mol电子,LiFePO4与硝酸反应转化为FePO4,Fe的化合价由+2价变为+3价,溶解1mol LiFePO4转移1mol电子,则转移0.3mol电子,溶解0.3mol LiFePO4,故答案为:0.3;
=0.1mol,产生1molNO,转移3mol电子,则生成0.1molNO转移0.3mol电子,LiFePO4与硝酸反应转化为FePO4,Fe的化合价由+2价变为+3价,溶解1mol LiFePO4转移1mol电子,则转移0.3mol电子,溶解0.3mol LiFePO4,故答案为:0.3;
(4)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3后,Li+的沉降率到99%,混合后溶液中含有的c(Li+)=![]() ,已知:Ksp(Li2CO3)=c2(Li+)·c(CO32-)=1.6×10-3,则滤液③中c(CO32-)=
,已知:Ksp(Li2CO3)=c2(Li+)·c(CO32-)=1.6×10-3,则滤液③中c(CO32-)= =
= =4 mol/L,故答案为:4;
=4 mol/L,故答案为:4;
(5)充电时,阳离子Li+移向阴极;放电时,正极发生还原反应,正极反应式为Li1-xFePO4+xLi++xe-=LiFePO4,故答案为:阴极;Li1-xFePO4+xLi++xe-=LiFePO4;
(6)①实验中加入HgCl2饱和溶液,可以发生反应:4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2,这样就可以使溶液中过量的Sn2+转化为稳定的络离子SnCl62-,从而防止用重铬酸钾溶液滴定溶液中Fe2+时干扰实验结果的测定,造成实验误差,故答案为:将溶液中过量Sn2+转化为稳定的SnCl62-,防止其干扰Fe2+的测定;
②根据6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O可知n(Fe2+)=6n(Cr2O72-)=![]() ,m(Fe)=
,m(Fe)=![]() ,所以铁的百分含量=
,所以铁的百分含量=  。
。


科目:高中化学 来源: 题型:
【题目】中美科学家在银表面首次获得了二维结构的硼烯,该科研成果发表在顶级刊物《Science》上,并获重点推荐,二维结构的硼烯如图所示。下列说法中错误的是( )
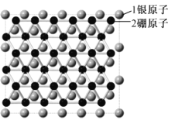
A.1.5mol硼原子核外电子数目为7.5NA
B.1个硼原子与其他原子最多只能形成3对共用电子对
C.硼的氧化物的水化物与NaOH溶液反应可生成BO2-
D.硼烯有望代替石墨烯作“硼烯-钠基”电池的负极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是熔点最高的金属,是重要的战略物资。自然界中钨主要存在于黑钨矿中,其主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含有少量Si、As的化合物。由黑钨矿冶炼钨的工艺流程如下:
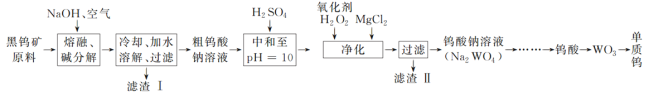
已知:①滤渣Ⅰ的主要成分是Fe2O3、MnO2;②上述流程中,钨的化合价只有在最后一步发生改变;③常温下钨酸溶于水。
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为______,请写出FeWO4在熔融条件下发生碱分解生成Fe2O3的化学方程式:_____________。
(2)上述流程中向粗钨酸钠溶液中加硫酸中和至pH=10后,溶液中的杂质阴离子含有SiO32—、HAsO32—、HAsO42—等,则“净化”过程中,加入H2O2时发生反应的离子方程式为HAsO32—+H2O2===HAsO42—+H2O,滤渣Ⅱ的主要成分是________。
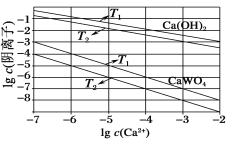
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度的升高而减小。如图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线。则:
①T1_____T2(填“>”或“<”);T1℃时Ksp(CaWO4)=______。
②向钨酸钠溶液中加入石灰乳会得到大量钨酸钙,发生反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。回答下列问题:
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61. 25 kJ,则该反应的热化学方程式为____。
(2)尾气中的NO2可以用烧碱溶液吸收的方法来处理,其中能生成NaNO2等物质,该反应的离子方程式为____。
(3)在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
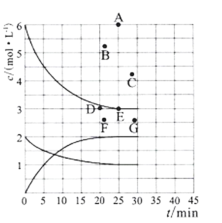
①下列能说明反应达到平衡状态的是____(选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4. 00 mol N2和12. 00 mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为 ___(选填字母)。
(4)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:![]()
测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 |
φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①计算0~20min时,v(N2O4)=____。
②已知该反应![]() ,其中k1、k2为速率常数,则373K时,
,其中k1、k2为速率常数,则373K时,![]() =_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
=_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物丙可由如图反应得到,则丙的结构不可能是

A. CH3CBr2CH2CH3B. (CH3)CBrCH2Br
C. CH3CH2CHBrCH2BrD. CH3(CHBr)2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:
mCeO2![]() (m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2
(m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2![]() mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
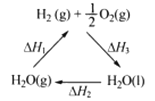
下列说法不正确的是
A. 该过程中CeO2没有消耗
B. 该过程实现了太阳能向化学能的转化
C. 右图中△H1=△H2+△H3
D. 以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水的固体,受热易分解,是生产电池、涂料以及感光材料的原材料。为探究纯净草酸亚铁晶体热分解的产物,设计装置图如下:
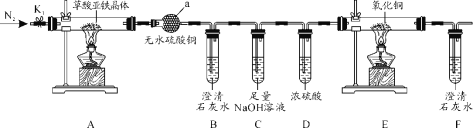
(1)仪器a的名称是______。
(2)从绿色化学考虑,该套装置存在的明显缺陷是_________。
(3)实验前先通入一段时间N2,其目的为__________。
(4)实验证明了气体产物中含有CO,依据的实验现象为_______。
(5)草酸亚铁晶体在空气易被氧化,检验草酸亚铁晶体是否氧化变质的实验操作是____。
(6)称取5.40g草酸亚铁晶体用热重法对其进行热分解,得到剩余固体质量随温度变化的曲线如下图所示:
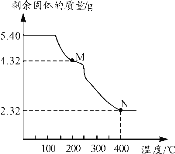
①上图中M点对应物质的化学式为_________。
②已知400℃时,剩余固体是铁的一种氧化物,试通过计算写出M→N发生反应的化学方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用制溴苯的废催化剂(主要含FeBr3及少量溴、苯)为原料,制取无水FeCl3和溴的苯溶液,选用的方法能达到相应实验目的的是

A. 用装置①及其试剂制取氯气
B. 用装置②氧化FeBr3溶液中的溴离子
C. 用装置③分离出FeCl3溶液,不能选用装置④分离
D. 用装置⑤将FeCl3溶液蒸发至干,可得无水FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是
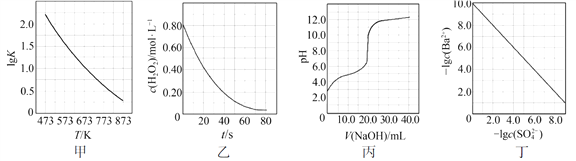
A. 图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
B. 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
C. 图丙是室温下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲线,说明HX是一元强酸
D. 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42)的关系曲线,说明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com