
| A. | 3.12g | B. | 4.28g | C. | 4.68g | D. | 5.08g |
分析 Mg和Cu在反应中失去电子,最终生成Mg(OH)2和Cu(OH)2,则可知镁,铜失去电子的物质的量等于生成沉淀需要的氢氧根的物质的量,根据生成气体NO的物质的量,可知反应转移电子的物质的量,结合氧化还原反应得失电子数目相等,可知最终生成沉淀的质量.
解答 解:反应中Cu$\stackrel{2{e}^{-}}{→}$Cu2+$\stackrel{2O{H}^{-}}{→}$Cu(OH)2,Mg$\stackrel{2{e}^{-}}{→}$Mg2+$\stackrel{2O{H}^{-}}{→}$Mg(OH)2,则可知镁,铜失去电子的物质的量等于生成沉淀需要的氢氧根的物质的量,
根据HNO3$\stackrel{+3{e}^{-}}{→}$NO,HNO3$\stackrel{+{e}^{-}}{→}$NO2,HNO3$\stackrel{+4{e}^{-}}{→}$N2O,生成0.224LNO转移的电子数为$\frac{0.224L}{22.4L/mol}×3$=0.03mol,生成0.224LN2O转移的电子数=0.08mol,共转移电子0.12mol,所以反应后生成沉淀的质量为2.24g+0.12mol×17g/mol=4.28g,
故选B.
点评 本题考查混合物的计算,题目难度中等,本题注意把握转移电子的数目与氢氧根离子之间的关系,为解答该题的关键.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ③⑥⑦ | B. | ①⑤⑥ | C. | ②③⑤ | D. | ④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 阳离子 | K+、Na+、Ba2+、NH4+ |
| 阴离了 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
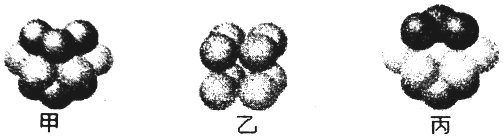
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
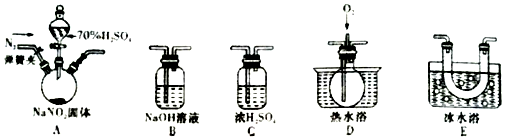
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
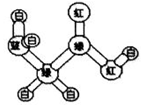 某期刊封面上有如下一个分子的球棍模型图:图中“棍”代表单键或双键或三键,不同颜色的球代表不同元素的原子.该模型图可代表一种( )
某期刊封面上有如下一个分子的球棍模型图:图中“棍”代表单键或双键或三键,不同颜色的球代表不同元素的原子.该模型图可代表一种( )| A. | 卤代羧酸 | B. | 酯 | C. | 氨基酸 | D. | 醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾与水反应,比钠与水反应更剧烈 | |
| B. | 砹(At)为深色固体,AgAt也难溶于水也不溶于稀硝酸 | |
| C. | 在空气中加热,铷(Rb)的氧化产物比钠的氧化产物更复杂 | |
| D. | HClO的酸性比H2CO3的酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com