
常温下,下列各组离子在指定溶液中一定能大量共存的是()
A. c(Al3+)=0.1mol/L的溶液中:Na+、K+、﹣、SO42﹣
B. 使酚酞呈红色的溶液中:K+、Ba2+、I﹣、NO3﹣
C. 由水电离出的c(H+)=1×10﹣13mol/L的溶液中:Na+、HCO3﹣、Cl﹣、Br﹣
D. 加入Al能放出H2的溶液中:Cl﹣、SO42﹣、NO3﹣、Mg2+
考点: 离子方程式的书写.
专题: 离子反应专题.
分析: A.﹣、Al3+之间发生双水解反应生成氢氧化铝沉淀;
B.使酚酞呈红色的溶液为碱性溶液,K+、Ba2+、I﹣、NO3﹣离子之间不发生反应;
C.由水电离出的c(H+)=1×10﹣13mol/L的溶液为酸性会碱性溶液,碳酸氢根离子与氢离子、氢氧根离子反应;
D.加入Al能放出H2的溶液为酸性或者碱性溶液,镁离子与氢氧根离子反应、酸性条件下硝酸根离子具有强氧化性,无法生成氢气.
解答: 解:A.﹣、Al3+离子之间发生双水解反应生成难溶物氢氧化铝,在溶液中不能大量共存,故A错误;
B.使酚酞呈红色的溶液中存在大量氢氧根离子,K+、Ba2+、I﹣、NO3﹣离子之间不反应,在溶液中能够大量共存,故B正确;
C.由水电离出的c(H+)=1×10﹣13mol/L的溶液中存在大量H+或OH﹣,HCO3﹣与H+、OH﹣反应,在溶液中不能大量共存,故C错误;
D.加入Al能放出H2的溶液中存在大量H+或OH﹣,Mg2+离子与氢氧根离子反应生成氢氧化镁沉淀,酸性溶液中NO3﹣具有强氧化性,无法生成氢气,在溶液中不能大量共存,故D错误;
故选B.
点评: 本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN﹣)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH﹣;溶液的颜色.


科目:高中化学 来源: 题型:
有关材料用途的说法中不正确的是 ( )。
A.氧化铝陶瓷可用作高压钠灯的灯管
B.氮化硅陶瓷可用作陶瓷发动机的材料
C.光导纤维可用作遥测遥控、照明等
D.氧化铝陶瓷可用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作中,能使电离平衡H2O⇌H++OH﹣,向右移动且溶液呈酸性的是( )
|
| A. | 向水中加入NaHSO4溶液 | B. | 向水中加入Al2(SO4)3溶液 |
|
| C. | 向水中加入NaOH溶液 | D. | 将水加热到100℃,使pH=6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在卤代烃R﹣CH2﹣CH2﹣X中化学键如图所示,则下列说法正确的是( )
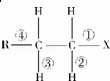
|
| A. | 发生水解反应时,被破坏的键是①和③ |
|
| B. | 发生消去反应时,被破坏的键是②和③ |
|
| C. | 发生水解反应时,被破坏的键是① |
|
| D. | 发生消去反应时,被破坏的键是①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产、生活、环境密切相关.下列说法错误的是()
A. 航天飞机上的隔热陶瓷瓦属于复合材料
B. 硫酸钠溶液和氯化钡溶液均能使蛋白质变性
C. “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化物有关
D. 绿色化学的核心是利用化学原理从源头上减少或消除工业生产对环境的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:
气体A的饱和溶液 A和食盐的饱和溶液
A和食盐的饱和溶液 悬浊液
悬浊液 晶体
晶体 纯碱
纯碱
则下列叙述错误的是()
A. A气体是CO2,B气体是NH3
B. 第Ⅲ步得到的晶体是发酵粉的主要成分
C. 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D. 第Ⅳ步操作的主要过程有溶解、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
(1)若A为氯碱工业的产品,C为厨房中的用品.
①反应Ⅲ的离子方程式是 .
②C浓度为0.1mol/L时,pH最接近 .
A.5.6 B.7.0 C.8.4 D.13.0
③B溶液中各离子浓度由大到小顺序是 ,氯碱工业中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1mol KI转移电子0.6mol,则三种物质间反应的离子方程式是 .
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料.
①检验某溶液中含有B的阳离子的方法是 .
②B可作净水剂,其原理是 (用方程式表示).在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是 .

查看答案和解析>>
科目:高中化学 来源: 题型:
为了检验某溴代烃中的溴元素,现进行如下操作,其中合理的是()
A. 取溴代烃少许,加入AgNO3溶液
B. 取溴代烃少许与NaOH水溶液共热,然后加入AgNO3溶液
C. 取溴代烃少许与NaOH乙醇溶液共热后,加入稀硝酸酸化后,再加入AgNO3溶液
D. 取溴代烃少许与NaOH水溶液共热后,加入稀硝酸酸化后,再加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
铝硅合金(含硅15.5%)在凝固时收缩率很小,因而这种合金适合铸造,现有下列3种晶体:①铝②硅③铝硅合金,它们的熔点从低到高的顺序是 ( )。
A.①②③ B.②①③ C.③②① D.③①②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com