
 2NH3(g)����H����92.6 kJ/mol��ʵ������ʼʱ���й����������ʾ��
2NH3(g)����H����92.6 kJ/mol��ʵ������ʼʱ���й����������ʾ��| ���� ��� | ��ʼʱ�����ʵ����ʵ���/mol | �ﵽƽ��ʱ�� ϵ�����ı仯 | ||
| N2 | H2 | NH3 | ||
| �� | 1 | 3 | 0 | �ų�������23.15 kJ |
| �� | 0.9 | 2.7 | 0.2 | �ų�������Q |
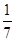
 2NH3(g)
2NH3(g)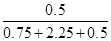 ��
��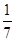 �����ڢٺ͢��н�����ƽ������ͬ�ģ�������������NH3�����������Ϊ
�����ڢٺ͢��н�����ƽ������ͬ�ģ�������������NH3�����������Ϊ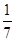 ��B��ȷ���ٺ͢ڽ���������ͬ��ƽ�⣬����N2ת��0.15 mol���ų�������Ϊ92.6 kJ/mol��0.15 mol��13.89 kJ��C����ȷ�������������Ϊ0.5 L������Ӧ�������ѹǿ��С��ƽ�����淴Ӧ�����ƶ�����ƽ��ʱ�ų�������С��23.15 kJ��D��ȷ��
��B��ȷ���ٺ͢ڽ���������ͬ��ƽ�⣬����N2ת��0.15 mol���ų�������Ϊ92.6 kJ/mol��0.15 mol��13.89 kJ��C����ȷ�������������Ϊ0.5 L������Ӧ�������ѹǿ��С��ƽ�����淴Ӧ�����ƶ�����ƽ��ʱ�ų�������С��23.15 kJ��D��ȷ��

 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ı䷴Ӧ�������ܸı仯ѧ��Ӧ���� |
| B���ӳ���ѧ��Ӧ��ʱ���ܸı仯ѧ��Ӧ���� |
| C�����淴Ӧ�ﵽ��ѧƽ��״̬ʱ������Ӧ���ʺ��淴Ӧ������� |
| D����ѧƽ��״̬��һ�־�ֹ״̬����Ӧ����������Ũ�Ȳ��ٸı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
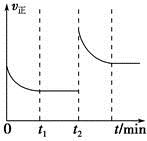
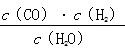 ����ش��������⡣
����ش��������⡣| A��v��(H2O)��v��(H2) |
| B�������������ƽ����Է�����������ʱ��ı� |
| C������n mol H2��ͬʱ����n mol CO |
| D�����������ʵ������ʵ�������ʱ��ı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��



 ����Ӧ�����У���������������ʱ��C�ڻ�����еĺ������¶ȣ�T���Ĺ�ϵ��ͼI��ʾ����Ӧ���ʣ�v����ѹǿ��p���Ĺ�ϵ��ͼII��ʾ����ͼ����������˵����ȷ���ǣ�������
����Ӧ�����У���������������ʱ��C�ڻ�����еĺ������¶ȣ�T���Ĺ�ϵ��ͼI��ʾ����Ӧ���ʣ�v����ѹǿ��p���Ĺ�ϵ��ͼII��ʾ����ͼ����������˵����ȷ���ǣ�������
| A��T1��T2��Q��0 |
| B������ѹǿ������B��ת�������� |
| C����Ӧ��ƽ�������������D��ƽ�������ƶ��� |
| D��a+b��c+d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g)��ƽ������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ��������ͼ�ش��������⣺
2SO3(g)��ƽ������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ��������ͼ�ش��������⣺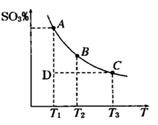
 2SO3(g)�ġ�H__________0���>����<������
2SO3(g)�ġ�H__________0���>����<������| A����ϵ���ܶȲ������仯 | B��SO2��SO3������ȱ��ֲ��� |
| C����ϵ����Ԫ�ص������ٷֺ������ٱ仯 | D����λʱ����ת��4 mol ���ӣ�ͬʱ����2 mol SO3 |
 2NH3(g)��ͼ1��ʾ�ڴ˷�Ӧ�����е������ı仯��ͼ2��ʾ��2L���ܱ������з�ӦʱN2�����ʵ�����ʱ��ı仯���ߡ�ͼ3��ʾ�������������������£��ı���ʼ�����������ʵ����Դ˷�Ӧƽ���Ӱ�졣
2NH3(g)��ͼ1��ʾ�ڴ˷�Ӧ�����е������ı仯��ͼ2��ʾ��2L���ܱ������з�ӦʱN2�����ʵ�����ʱ��ı仯���ߡ�ͼ3��ʾ�������������������£��ı���ʼ�����������ʵ����Դ˷�Ӧƽ���Ӱ�졣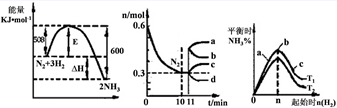
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3OH(g)��H2O(g)��5 min��Ӧ�ﵽƽ��ʱc(CH3OH)Ϊ0.2 mol��L��1��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶ȹ�ϵ��ͼ��ʾ������˵���������(����)��
CH3OH(g)��H2O(g)��5 min��Ӧ�ﵽƽ��ʱc(CH3OH)Ϊ0.2 mol��L��1��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶ȹ�ϵ��ͼ��ʾ������˵���������(����)��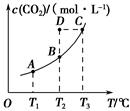
| A��0��5 min��CO2��ƽ����Ӧ����Ϊ0.04 mol��(L��min)��1 |
B����ӦCO2(g)��3H2(g) CH3OH(g)��H2O(g)�Ħ�H��0 CH3OH(g)��H2O(g)�Ħ�H��0 |
| C����T2��ʱ������Ӧ����״̬D����һ����v����v�� |
| D����T1�桢T2��ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ˮ��ˮϡ�ͺ���Һ��c(NH3��H2O) /c(NH4��)��ֵ��С |
| B��һ�������£�ʹ�ô����ܼӿ췴Ӧ���ʲ���߷�Ӧ���ƽ��ת���� |
| C�������£�2NO(g)��O2(g)��2NO2(g)�ܹ��Է����У���÷�Ӧ�ġ�H��0 |
| D����ͬ�����£�Na2CO3��Һ�ļ���ǿ��C6H5ONa��˵��C6H5OH������ǿ��H2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
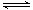 4NO2(g)��O2(g) ���SH��0
4NO2(g)��O2(g) ���SH��0| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol��L��1 | 5.00 | 3.52 | 2.48 |
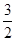 ��(������NO2�ۺϳ�N2O4)����N2O5��ת����a1�� �����¶��·�Ӧ��ƽ�ⳣ��K��_______��
��(������NO2�ۺϳ�N2O4)����N2O5��ת����a1�� �����¶��·�Ӧ��ƽ�ⳣ��K��_______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com