
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
分析 (1)依据燃烧热概念是1mol可燃物完全燃烧生成稳定氧化物放出的热,结合热化学方程式书写方法写出,标注物质聚集状态和对应焓变;
(2)反应的焓变=反应物键能总和-生成物键能总和;
(3)A.某温度下纯水中的c(H+)=10-6,氢离子能的和氢氧根离子浓度相同;
B.依据沉淀溶解平衡分析判断;
C.相同温度下,铵盐溶液中铵根微弱水解,0.1mol•L-1NH4Cl溶液中,铵根离子浓度略小于0.1mol/L,氨水是弱电解质存在电离平衡,溶液中NH4+的浓度远远小于0.1mol/L;
D.碳酸根离子水解程度大于碳酸氢根离子分析判断;
E.向饱和石灰水中加入CaO固体,氧化钙和水反应生成氢氧化钙,析出氢氧化钙,溶液中Ca2+、OH-的物质的量均减小.
解答 解:(1)在25℃、101kPa下,1g乙烷燃烧生成CO2和液态水时放热QkJ,1mol乙烷(质量为30g)燃烧生成二氧化碳和液态水放热30QKJ热量,则表示乙烷燃烧热的热化学方程式为C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-30QkJ/mol,
故答案为:C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-30QkJ/mol;
(2)反应的焓变=反应物键能总和-生成物键能总和,△H=4×414kJ/mol+×158kJ/mol-(4×489kJ/mol+4×565kJ/mol)=-1928kJ/mol,即△H=-1928kJ/mol,
故答案为:-1928kJ/mol;
(3)A.某温度下纯水中的c(H+)=10-6,氢离子能的和氢氧根离子浓度相同,仍然呈中性,故A错误;
B.依据沉淀溶解平衡分析判断,银离子浓度和氯离子浓度乘积为常数,用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小,故B正确;
C.相同温度下,铵盐溶液中铵根微弱水解,0.1mol•L-1NH4Cl溶液中,铵根离子浓度略小于0.1mol/L,氨水是弱电解质存在电离平衡,溶液中NH4+的浓度远远小于0.1mol/L,相同温度下,0.1mol•L-1NH4Cl溶液中NH4+的浓度比0.1mol•L-1氨水中NH4+的浓度大,故C正确;
D.碳酸根离子水解程度大于碳酸氢根离子,相同温度下,pH均为8的Na2CO3和NaHCO3溶液,后者物质的量浓度大,故D错误;
E.向饱和石灰水中加入CaO固体,氧化钙和水反应生成氢氧化钙,析出氢氧化钙,溶液中Ca2+、OH-的物质的量均减小,故E正确;
故答案为:AD.
点评 本题考查了热化学方程式的书写方法,燃烧热概念分析应用,水的电离,盐类水解,弱电解质电离平衡的分析判断是解题关键,题目难度中等.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 体系压强保持不变 | B. | 混合气体颜色保持不变 | ||
| C. | SO3和NO的体积比保持不变 | D. | 每消耗1molSO3的同时生成1molNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g O2中含有的氧分子数为NA | |
| B. | 1mol Zn变为Zn2+时失去的电子数目为NA | |
| C. | 常温常压下,11.2 L H2中含有的氢分子数为0.5NA | |
| D. | 1L 1 mol•L-1 BaCl2溶液中含有的钡离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3→CO2 | B. | HClO→O2 | C. | HCl(浓)→MnCl2 | D. | NaBr→NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
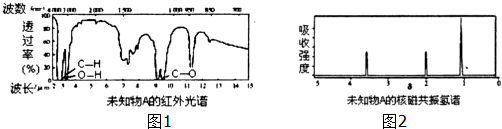
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com