
现拟分离乙酸乙酯、乙酸、乙醇的混合物,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法,在方框内填入所分离的有关物质的结构简式。

科目:高中化学 来源: 题型:
过氧化氢和臭氧是用途很广的氧化剂。试回答下列问题:
(1) 过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:
(2) Na2O2 、K2O2、 以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最适合的过氧化物是____________(写电子式),
(3) 臭氧(O3)可以使湿润的淀粉-碘化钾试纸变蓝,反应的化学方程式为:
KI+O3+H2O→KOH+I2+O2(未配平 ) 回答问题:
① 还原产物的化学式为
② 配平后的化学方程式是
(4)O3 可由臭氧发生器(原理如图8所示)电解稀硫酸制得。
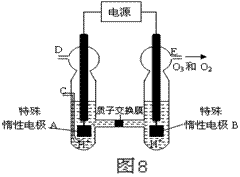

①图中阴极为 (填“A”或“B”)。
② 若C处不通入O 2 ,D、E处分别收集到11.2L和4.48L
气体(标准状况下), 则E处收集的气体中O3所占的体积分数
为 (忽略 O 3 的分解)。
③ 若C处通入O 2,则A极的电极反应式为: 。
(5)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
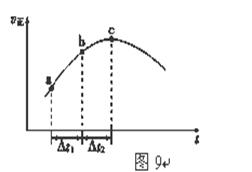
a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.反应物的总能量低于生成物的总能量
d.Δt1=Δt2时,NO的转化率:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)利用H2S废气来制取氢气的方法有多种。
①高温热分解法。
已知:H2S(g) H2(g)+S2(g)
H2(g)+S2(g)
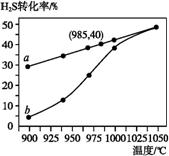
在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L -1测定H2S的
-1测定H2S的 转化率,结果见下图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不
转化率,结果见下图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不 同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985 ℃时H2S按上述反应分解的平衡常数K= ;说明温度升高,曲线b向曲线a逼近的原因: 。
同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985 ℃时H2S按上述反应分解的平衡常数K= ;说明温度升高,曲线b向曲线a逼近的原因: 。
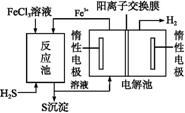
②电化学法。
该法制氢过程的示意图如下。反应池中反应物的流向采用气、液逆流方式,其目的是 ;反应池中发生反应的化学方程式为 。反应后的溶液进入电解池,电解总反应的离子方程式为 。
(2)氯碱工业中电解饱和食盐水的原理示意图如下图所示。
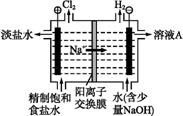
①溶液A的溶质是 ;
②电解饱和食盐水的离子方程式是 ;
③电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学研究性小组采用如下装置(夹持和加热仪器已略去)电解饱和食盐水一段时间,并通过实验测定产物的量来判断饱和食盐水的电解率。
饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%
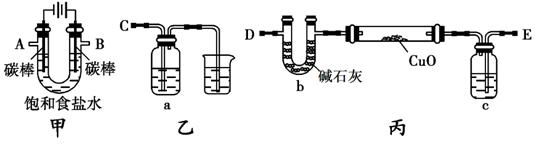
甲方案:利用甲、乙装置测定饱和食盐水的电解率,
(1)若饱和食盐水中滴有酚酞,则电解过程中甲装置中的实验现象:
(2)若洗气瓶a中盛放的为足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率,则正确的连接顺序为 连________(填A、B、C、D、E等导管口),则洗气瓶a中发生反应的离子方程式为
乙方案:利用甲、丙装置测定饱和食盐水的电解率,
(3)对于乙方案,有同学提出有两种方法都可测得饱和食盐水的电解率,
Ⅰ.通过测定硬质玻璃管中氧化铜固体前后质量差来计算饱和食盐水的电解率
Ⅱ.通过测定丙装置中除硬质玻璃管外的某装置前后质量差来计算饱和食盐水的电解率
①.一同学认为可以在乙方案方法Ⅱ中的装置中添加一干燥装置防止外界空气中的水蒸气的干扰,则该干燥装置应与 口连接
a.A b.B c.D d.E
②.另一同学认为乙方案的方法Ⅰ、Ⅱ测得的实验结论都不正确,你是否同意?请说明理由
丙方案:只利用甲装置测定饱和食盐水的电解率。
(4)若电解150mL饱和食盐水一段时间,测得溶液的为pH为14,求饱和食盐水的电解率
(假设电解前后溶液体积不变,饱和食盐水密度约为1.33 g/mL,溶解度为36.0g)。
(5)若往该电解后所得溶液中通入二氧化碳气体2.24L(标准状况),则所得溶液中各离子浓度大小关系为:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物的一氯取代物的同分异构体数目相等的是( )
①2,3,4三甲基己烷 ②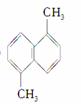 ③2,3,4三
③2,3,4三
甲基戊烷 ④间甲基乙苯
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验设计和结论相符的是
A.加入NaOH溶液并加热,能产生使湿润红色石蕊试纸变蓝气体,则一定含有NH4+
B.将SO2通入溴水,溴水褪色,说明SO2具有漂白性
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
D.在含FeC12杂质的FeCl3溶液中通入足里C12后,充分加热除去过量的C12,即可得到较纯净的FeC13溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
.下列判断正确的是( )
A.酸酐一定是氧化物 B.晶体中一定存在化学键
C.碱性氧化物一定是金属氧化物 D.正四面体分子中键角一定是109o28′
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com