
| A. | 原子最外层电子数由少到多的顺序:X=W<Y<Z | |
| B. | 原子半径由大到小的顺序:r(W)>r(X)>r(Y)>r(Z) | |
| C. | 元素非金属性由强到弱的顺序:X、Y、W | |
| D. | 元素的简单气态氢化物的稳定性由强到弱的顺序:Y、X、W |
分析 短周期主族元素X、Y、Z、W原子序数依次增大,X元素的单质可在自然界中形成最硬的矿石,该矿石为金刚石,则X为C元素,Z元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质,则Z为Mg元素,Y原子最外层有6个电子,而且原子序数比Mg小,则Y为O元素,W与C同主族,则W为Si元素,据此解答.
解答 解:短周期主族元素X、Y、Z、W原子序数依次增大,X元素的单质可在自然界中形成最硬的矿石,该矿石为金刚石,则X为C元素,Z元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质,则Z为Mg元素,Y原子最外层有6个电子,而且原子序数比Mg小,则Y为O元素,W与C同主族,则W为Si元素,
A.原子最外层电子数由少到多的顺序:Z<W=X<Y,故A错误;
B.同周期自左而右原子半径减小,同主族从上到下原子半径增大,则原子半径由大到小的顺序:r(Z)>r(W)>r(X)>r(Y),故B错误;
C.X为碳元素,Y为O元素,W为Si元素,则元素非金属性由强到弱的顺序:Y、X、W,故C错误;
D.元素的非金属性越强,其氢化物的稳定性越强,非金属性:O>C>Si,则气态氢化物的稳定性由强到弱的顺序:Y、X、W,故D正确;
故选D.
点评 本题考查结构性质位置关系应用,题目难度中等,正确推断各元素为解答关键,注意熟练掌握元素周期表结构、元素周期律内容,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
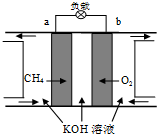 全球气候变暖已经成为全世界人类面临的重大问题.
全球气候变暖已经成为全世界人类面临的重大问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸溶液与氢氧化钡溶液反应:H++SO42-+OH-+Ba2+═H2O+BaSO4↓ | |
| B. | 氯气溶于水:H2O+Cl2═2H++ClOˉ+Clˉ | |
| C. | 金属钠投入水中:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 向氯化铝溶液中加入足量氨水:A13++4NH3•H2O═AlO2-+2H2O+4NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
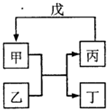 甲乙丙丁戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足右图转化关系的是( )
甲乙丙丁戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足右图转化关系的是( ) | 甲 | 乙 | 丙 | 戊 | |
| A | NH3 | Cl2 | N2 | H2 |
| B | C | SiO2 | CO | CuO |
| C | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | CO2 |
| D | 乙醇乙酯 | NaOH溶液 | 乙醇 | 乙酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子是由原子核和核外电子构成的 | |
| B. | 保持水的化学性质的粒子是水分子 | |
| C. | 分子的质量总比原子的质量大 | |
| D. | 在化学反应中分子可分而原子不可分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH═CH3COO-+H+ | B. | NaOH═Na++OH- | ||
| C. | H2SO4═H++SO42- | D. | KClO3═K++Cl-+3O2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com