
分析 ①16g肼为0.5mol,所以1mol肼燃烧放热709.68KJ,据已知条件书写热化学方程式;
②1molNa2SO3和N2H4反应,转移电子分别为2mol和4mol,据电子守恒解答;
解答 解:①16g肼为0.5mol,所以1mol肼燃烧放热709.68KJ,热化学方程式为:N2H4(1)+O2(g)=N2(g)+2H2O(1);△H=-709.74kJ•mol-1,
故答案为:N3H4(1)+O2(g)=N2(g)+2H2O(1);△H=-709.74kJ•mol-1;
②1molNa2SO3和N2H4被氧化,转移电子分别为2mol和4mol,除去等质量的O2,消耗Na2SO3和N2H4的物质的量之比为2:1,质量比为:$\frac{126g×2}{32g}$=$\frac{63}{8}$,
故答案为:63:8;
点评 本题考查了热化学方程式书写、氧化还原反应中的电子守恒计算,掌握基础是关键,题目难度中等.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 盐酸、硫酸、五水硫酸铜 | B. | NH3、Cu、空气 | ||
| C. | NaOH、SO2、空气 | D. | 氨水、食盐、酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是( )
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是( )| A. | 从实验装置上看,除了缺少环形玻璃搅拌棒外没有其他问题 | |
| B. | 大烧杯上如不盖硬纸板,测得的中和热数值会偏大 | |
| C. | 用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会偏大 | |
| D. | 实验中改用60 mL 0.50 mol•L-1盐酸跟50 mL 0.55 mol•L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量不相等,但是所求中和热相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀HCl | B. | 饱和NaOH溶液 | C. | FeCl3溶液 | D. | CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1molAlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 | |
| B. | 28 g乙烯分子中含有极性共价键的数目为6NA | |
| C. | 50mL18mol/L浓硫酸与足量的铜反应,生成SO2的分子数小于0.45NA | |
| D. | 足量的铁与0.1molC12充分反应,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
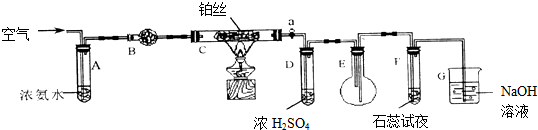
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,35Cl、37Cl之间的关系是同位素.
,35Cl、37Cl之间的关系是同位素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “垃圾不落地,台州更美丽” | B. | 太阳能热水器代替燃气热水器 | ||
| C. | 杜绝使用一切燃料 | D. | 环保袋代替一次性塑料袋 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com